题目内容
17.如图实验操作正确的是( )| A. | 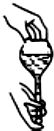 检验容量瓶是否漏水 | B. |  稀释浓硫酸 | ||
| C. |  蒸发 | D. |  过滤 |
分析 A.根据容量瓶查漏的方法:加水、盖塞子、倒转、旋塞、倒转来回答;
B.稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中;
C.蒸发需要用玻璃棒不断搅拌;
D.过滤液体时,要注意“一贴、二低、三靠”的原则.
解答 解:A.容量瓶查漏的方法:往容量瓶中加水,塞好瓶塞,将容量瓶倒过来,若不漏水,将瓶塞旋转180°,再倒过来,看是否漏水,故A正确;
B.稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中,故B错误;
C.蒸发需要用玻璃棒不断搅拌,防止液体飞溅,故C错误;
D.漏斗下端应紧靠烧杯内壁,故D错误.
故选A.
点评 本题考查较为综合,涉及基础实验操作,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握实验的方法、步骤和使用的仪器,注重相关基础知识的积累,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.若NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1mol OH-含有的电子数为9NA | |
| B. | 常温常压下,NO2和N2O4的混合物23g中含有NA个氧原子 | |
| C. | 标准状况下,2.8gN2和2.24L CO所含电子数均为1.4NA | |
| D. | 标准状况下,22.4 L 乙醇中含有NA个乙醇分子 |
8.证明NaHSO3溶液中HSO3-的电离程度大于水解程度,可采用的实验方法是( )
| A. | 加入盐酸 | B. | 加入Ba(OH)2溶液 | C. | 测定溶液的pH值 | D. | 加入品红溶液 |
5.入冬以来,东北各地陆续出现大范围的雾霾天气,主要原因是由于大气中PM2.5含量升高所造成的,PM2.5是指大气中直径小于或等于2.5微米(1微米=10-6米)的颗粒物.其中PM2.5的主要来源与汽车排放的尾气有关.下列有关叙述正确的是( )
| A. | 胶体区别于其它分散系的本质特征是具有丁达尔现象 | |
| B. | 将直径等于2.5微米的颗粒物分散于水即成为胶体 | |
| C. | 雾具有丁达尔现象 | |
| D. | 增加使用汽车,提高交通效率可缓解雾霾天气的产生 |
12.酸性条件下,高锰酸钾与草酸钾反应的离子方程为:MnO4-+C2O42-+H+→CO2↑+Mn2++ .关于此反应的叙述正确的是( )
| A. | 配平该反应后,H+的系数是8 | B. | 该反应右边方框内的产物是OH- | ||
| C. | 该反应电子转移总数是5e- | D. | 该反应的还原剂是C2O42- |
2.下列溶液中物质的量浓度为1mol•L-1的是( )
| A. | 将20 g NaOH 溶解在500mL 水中 | |
| B. | 将22.4 L HCl 气体溶于水配成1 L 溶液 | |
| C. | 将1 L 10 mol•L-1浓盐酸加入9 L 水中 | |
| D. | 将10 g NaOH 溶解在少量水中,恢复至室温,再加蒸馏水直到溶液体积为250 mL |
9.肼(N2H4)是火箭发动机的一种燃料,反应时N2O4为氧化剂,反应生成N2和水蒸气.
已知:N2(g)+2O2(g)═N2O4(g);△H=+a kJ/mol
N2H4(g)+O2(g)═N2(g)+2H2O(g);△H=-b kJ/mol
下列表示肼和N2O4反应的热化学方程式,正确的是( )
已知:N2(g)+2O2(g)═N2O4(g);△H=+a kJ/mol
N2H4(g)+O2(g)═N2(g)+2H2O(g);△H=-b kJ/mol
下列表示肼和N2O4反应的热化学方程式,正确的是( )
| A. | 2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g);△H=-(b+a) kJ/mol | |
| B. | 2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g);△H=-(2b+a)kJ/mol | |
| C. | 2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g);△H=-(a-2b) kJ/mol | |
| D. | 2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g);△H=-(b-a) kJ/mol |
7.设阿伏加德罗常数的数值为NA,下列说法正确的是( )
| A. | 室温下体积为10L、pH=13的NaOH溶液中含有OH-的数目为NA | |
| B. | 常温常压下,17g氨气中含有氢原子的数目为NA | |
| C. | PH=1的醋酸溶液中,醋酸分子的个数为NA | |
| D. | 体积为1L、物质的量浓度为1mol•L-1的Na2CO3溶液中含有NA个CO32- |