题目内容
(1)普通锌锰干电池的结构如图所示。回答下列问题。
①电池中电解质溶液为________。
②正极反应式为________。
③放电时,NH4+向________(填“正极”或“负极”)移动。
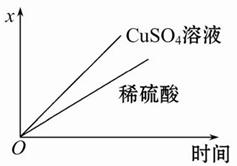
(2)废电池中的锌皮常用于实验室制氢气,废锌皮和纯锌粒分别与同浓度的稀硫酸反应,产生氢气速率较大的是________,原因是________________________。
若用过量的纯锌粒与一定量的稀硫酸反应,为了加快反应速率又不影响产生氢气的量,下列措施可行的是________(填序号)。
| A.微热 |
| B.加入适量氧化铜 |
| C.加入少量硫酸铜溶液 |
| D.加水 |
(1)①NH4Cl(或氯化铵)溶液 ②2MnO2+2NH4++2e-=Mn2O3+H2O+2NH3 ③正极
(2)废锌皮 废锌皮在稀硫酸中可构成原电池,加快负极失电子速率,相应产生氢气速率较大 AC
解析

练习册系列答案
相关题目
如下图所示,用铅蓄电池电解100 g 10.0%的硫酸钠溶液,经过一段时间后,测得溶液质量变为95.5 g。下列说法正确的是( )
| A.电路中转移0.25 mol电子 |
| B.铅蓄电池中消耗0.5 mol H2SO4 |
| C.铅蓄电池的负极反应式为:PbSO4+2H2O-2e-=PbO2+4H++SO |
| D.Fe电极发生的电极反应为Fe-2e-=Fe2+ |






 2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4 mol 电子时铁电极的质量减少11.2 g。请回答下列问题。
2PbSO4+2H2O,现用如图装置进行电解(电解液足量),测得当铅蓄电池中转移0.4 mol 电子时铁电极的质量减少11.2 g。请回答下列问题。