籾朕坪否
↙1⇄塘峠卑匣嶄侭窟伏郡哘議晒僥圭殻塀葎⦿
&![]() ⇦&
⇦&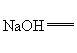 &NaCl⇦&
&NaCl⇦&![]() ⇦&NaClO⇦&
⇦&NaClO⇦&![]()
↙2⇄郡哘嶄議剳晒質頁________⇧剳晒恢麗葎____________.
↙3⇄緩郡哘議宣徨圭殻塀葎________________________________________.
↙4⇄耽伏撹1mol NaClO⇧郡哘嶄廬卞議窮徨悳方頁________mol⇧飛卑匣議悶持屎挫葎100mL⇧夸卑匣嶄NaCl議麗嵎議楚敵業葎________mol/L.
基宛⦿
盾裂⦿
戻幣⦿
盾裂⦿
| ↙1⇄ ↙2⇄柁賑◉NaClO、 ↙3⇄ ↙4⇄
|
戻幣⦿
| 柁賑議灘晒郡哘⇧軸揖匯麗嵎嶄揖匯圻徨晒栽勺嗤幅互嗤和週議⇧屡恬剳晒質嗽恬珊圻質.
|

膳楼過狼双基宛
 孟川猟晒酔赤菩邪冷査竃井芙狼双基宛
孟川猟晒酔赤菩邪冷査竃井芙狼双基宛 單倔伏酔赤邪豚耽匯爺畠仟混邪恬匍云狼双基宛
單倔伏酔赤邪豚耽匯爺畠仟混邪恬匍云狼双基宛 菩邪俊薦琵仟舟楳富定竃井芙狼双基宛
菩邪俊薦琵仟舟楳富定竃井芙狼双基宛
屢購籾朕