题目内容
16.己知X、Y、Z、W、N、U、V是短周期的主族元素,原子序数依次增大.X与N同主族,且与W都能形成A2B、A2B2型化合物;Z、W的单质常温下均为无色气体;Y原子的L层电子数是K层电子数的2倍;U原子的最外层电子数是其电子层数的2倍,试回答下列问题:(1)YW2的电子式
 ;V原子的结构示意图
;V原子的结构示意图 ;Z的氢化物结构式为
;Z的氢化物结构式为 ;写出U元素在周期表中的位置第三周期VIA族;N2W2中含有的化学键有离子键、共价键(化学键类型)
;写出U元素在周期表中的位置第三周期VIA族;N2W2中含有的化学键有离子键、共价键(化学键类型)(2)X、Y、Z、W四种元素(按顺序)可组成原子个数比为5:1:1:3的化合物,该化合物的稀溶液与足量氢氧化钠溶液反应的离子方程式为NH4++HCO3-+2OH-=NH3.H2O+CO32-.
分析 X、Y、Z、W、N、U、V是短周期的主族元素,原子序数依次增大.Y原子的L层电子数是K层电子数的2倍,则L层电子数为4,故Y为C元素;Z、W的单质常温下均为无色气体,结合原子序数可知Z为N元素、W为O元素;X与N同主族,且与W都能形成A2B、A2B2型化合物,则X为H元素、N为Na元素;U、V处于第三周期,U原子的最外层电子数是其电子层数的2倍,最外层电子数为6,故U为S元素,则V为Cl,据此解答.
解答 解:X、Y、Z、W、N、U、V是短周期的主族元素,原子序数依次增大.Y原子的L层电子数是K层电子数的2倍,则L层电子数为4,故Y为C元素;Z、W的单质常温下均为无色气体,结合原子序数可知Z为N元素、W为O元素;X与N同主族,且与W都能形成A2B、A2B2型化合物,则X为H元素、N为Na元素;U、V处于第三周期,U原子的最外层电子数是其电子层数的2倍,最外层电子数为6,故U为S元素,则V为Cl.
(1)YW2为CO2,电子式为 ;V为Cl元素,原子的结构示意图为
;V为Cl元素,原子的结构示意图为 ;
;
Z的氢化物为NH3,结构式为 ;U为S元素,在周期表中的位置:第三周期VIA族;Na2O2中含有的化学键有:离子键、共价键;
;U为S元素,在周期表中的位置:第三周期VIA族;Na2O2中含有的化学键有:离子键、共价键;
故答案为: ;
; ;
; ;第三周期VIA族;离子键、共价键;
;第三周期VIA族;离子键、共价键;
(2)H、C、N、O四种元素(按顺序)可组成原子个数比为5:1:1:3的化合物,该化合物为NH4HCO3,NH4HCO3的稀溶液与足量氢氧化钠溶液反应的离子方程式为:NH4++HCO3-+2OH-=NH3.H2O+CO32-,
故答案为:NH4++HCO3-+2OH-=NH3.H2O+CO32-.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,侧重对化学用语的考查,难度不大.

练习册系列答案
相关题目
11.取两份等质量的铝份和铁粉,分别与足量的盐酸反应,在相同状态下产生的气体体积之比是( )
| A. | 1:1 | B. | 3:2 | C. | 28:9 | D. | 2:3 |
7.FeCl3在现代工业生产中应用广泛.某化学研究性学习小组模拟工业流程制备无水FeCl3,再用副产品FeCl3溶液吸收有毒的H2S.
Ⅰ.经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华.他们设计了制备无水 FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
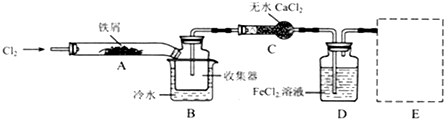
①检验装置的气密性;
②通入干燥的Cl2,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成;
④…
⑤体系冷却后,停止通入Cl2,并用干燥的H2赶尽Cl2,将收集器密封.
请回答下列问题:
(1)装置A中反应的化学方程式为2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3.
(2)操作步骤中,为防止FeCl3潮解所采取的措施有(填步骤序号)②⑤.
(3)如果没有装置C的设计,会导致D装置中水挥发到接受器,使FeCl3潮解.
(4)用离子方程式表示虚线框E中所增加装置和试剂的作用: 、Cl2+2OH-=Cl-+ClO-+H2O.
、Cl2+2OH-=Cl-+ClO-+H2O.
(5)用装置D中的副产品FeCl3溶液吸收H2S,得到单质硫,请写出反应的离子方程式:2Fe3++2H2S=2Fe2++2H++S↓.
Ⅱ.反应结束后,将收集器中所得固体完全溶于稀盐酸,小组同学对所得溶液金属阳离子的成分有三种观点:①只有Fe3+;②只有Fe2+;③既有Fe3+又有Fe2+.
为探究溶液的组成,实验如下:
综合上述实验分析,所得溶液中含有的金属阳离子有Fe3+、Fe2+.
Ⅰ.经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华.他们设计了制备无水 FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:

①检验装置的气密性;
②通入干燥的Cl2,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成;
④…
⑤体系冷却后,停止通入Cl2,并用干燥的H2赶尽Cl2,将收集器密封.
请回答下列问题:
(1)装置A中反应的化学方程式为2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3.
(2)操作步骤中,为防止FeCl3潮解所采取的措施有(填步骤序号)②⑤.
(3)如果没有装置C的设计,会导致D装置中水挥发到接受器,使FeCl3潮解.
(4)用离子方程式表示虚线框E中所增加装置和试剂的作用:
 、Cl2+2OH-=Cl-+ClO-+H2O.
、Cl2+2OH-=Cl-+ClO-+H2O.(5)用装置D中的副产品FeCl3溶液吸收H2S,得到单质硫,请写出反应的离子方程式:2Fe3++2H2S=2Fe2++2H++S↓.
Ⅱ.反应结束后,将收集器中所得固体完全溶于稀盐酸,小组同学对所得溶液金属阳离子的成分有三种观点:①只有Fe3+;②只有Fe2+;③既有Fe3+又有Fe2+.
为探究溶液的组成,实验如下:
| 实验步骤 | 实验现象 | 实验结论及反应离子方程式 |
| ①取少量所得溶液于试管中,加入少量KSCN溶液. | 溶液中出现红色. | 说明:假设②不成立,假设①或③成立; 反应的离子方程式是Fe3++3SCN-=Fe(SCN)3. |
| ②另取少量所得溶液于试管中,加入少量酸性 KMnO4溶液. | 溶液紫红色退去 | 说明:假设②或③成立. |
8.下列说法中,不正确的是( )
| A. | 可利用过滤的方法分离胶体和溶液 | |
| B. | 胶体中分散质粒子直径大小在1~100nm之间 | |
| C. | 可以利用丁达尔效应区分胶体和溶液 | |
| D. | 胶体在一定条件下能稳定存在 |
6. 三乙酸甘油酯是一种优良的溶剂、定香剂和增塑剂.实验室制备三乙酸甘油酯的反应原理、实验装置及相关数据如下:3CH3COOH+
三乙酸甘油酯是一种优良的溶剂、定香剂和增塑剂.实验室制备三乙酸甘油酯的反应原理、实验装置及相关数据如下:3CH3COOH+ $?_{△}^{浓H_{2}SO_{4}}$
$?_{△}^{浓H_{2}SO_{4}}$ +3H2O
+3H2O
实验步骤:
步骤1.在500mL反应器中加入200g冰醋酸,92g甘油和100mL苯,开动搅拌器,慢慢从插温度计口加入3mL浓硫酸后,缓缓加热并回流1h,停止加热.
步骤2.用5%碳酸钠溶液洗涤,再用水洗涤,最后加入无水氯化钙.
步骤3.先进行常压蒸馏收集75~85℃馏分.
步骤4.将常压馏分再进行减压蒸馏,收集128~131℃/933Pa馏分,最终得产品176g.
(1)步骤1先开搅拌器后加浓硫酸的目的是防止局部浓硫酸浓度过大,造成有机物脱水炭化;冰醋酸过量的目的是有利于向酯化方向移动,提高甘油的转化率
(2)用5%碳酸钠溶液洗涤的主要目的是除去产品的硫酸、乙酸;加无水氯化钙的目的是除去有机物中的水份
(3)最后用减压蒸馏而不用常压蒸馏其原因是防止常压蒸馏温度过高导致产品分解
(4)本次实验产率为80.7%.
 三乙酸甘油酯是一种优良的溶剂、定香剂和增塑剂.实验室制备三乙酸甘油酯的反应原理、实验装置及相关数据如下:3CH3COOH+
三乙酸甘油酯是一种优良的溶剂、定香剂和增塑剂.实验室制备三乙酸甘油酯的反应原理、实验装置及相关数据如下:3CH3COOH+ $?_{△}^{浓H_{2}SO_{4}}$
$?_{△}^{浓H_{2}SO_{4}}$ +3H2O
+3H2O| 物质 | 相对 分子质量 | 密度/g•cm-3 | 沸点/℃ | 水中 溶解性 |
| 甘油 | 92 | 1.2636 | 290 (分解) | 溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 三乙酸甘油酯 | 218 | 1.1596 | 258 | 不溶 |
步骤1.在500mL反应器中加入200g冰醋酸,92g甘油和100mL苯,开动搅拌器,慢慢从插温度计口加入3mL浓硫酸后,缓缓加热并回流1h,停止加热.
步骤2.用5%碳酸钠溶液洗涤,再用水洗涤,最后加入无水氯化钙.
步骤3.先进行常压蒸馏收集75~85℃馏分.
步骤4.将常压馏分再进行减压蒸馏,收集128~131℃/933Pa馏分,最终得产品176g.
(1)步骤1先开搅拌器后加浓硫酸的目的是防止局部浓硫酸浓度过大,造成有机物脱水炭化;冰醋酸过量的目的是有利于向酯化方向移动,提高甘油的转化率
(2)用5%碳酸钠溶液洗涤的主要目的是除去产品的硫酸、乙酸;加无水氯化钙的目的是除去有机物中的水份
(3)最后用减压蒸馏而不用常压蒸馏其原因是防止常压蒸馏温度过高导致产品分解
(4)本次实验产率为80.7%.
 HCN+OH-
HCN+OH-