题目内容
 已知2SO2 (g)+O2(g)
已知2SO2 (g)+O2(g) 2SO3(g)△H=-196kJ?mol-1,5000C时将2mol SO2和1molO2装入一体积恒定的10L密闭容器中,2分钟(t1)时达到平衡.如下图所示:
2SO3(g)△H=-196kJ?mol-1,5000C时将2mol SO2和1molO2装入一体积恒定的10L密闭容器中,2分钟(t1)时达到平衡.如下图所示:请回答下列问题:
(1)用O2表示2分钟内该反应的平均反应速率为
0.045
0.045
mol?L-1?min-1.计算500℃时该反应的平衡常数K=
8.1×103
8.1×103
mol?L-1)-1(2)在上述条件下起始装入的SO2和O2各2mol,达到平衡后设SO2的转化率为x,列出求x的方程
| (0.2x)2 |
| (0.2-0.2x)2(0.1-0.1x) |
| (0.2x)2 |
| (0.2-0.2x)2(0.1-0.1x) |
(3)某温度时,该反应的平衡常数K=800(mol?L-1)-1,则该温度
>
>
500℃(填“>”、“<”、“=”).分析:(1)根据v=
计算反应速率;根据K=
计算平衡常数;
(2)用x表示出平衡时SO3、SO2和O2的浓度,代入K=
列式;
(3)根据常数的相对大小,判断平衡移动方向,再由温度对化学平衡影响判断.
| △c |
| △t |
| c2(SO3) |
| c2(SO2)c(SO2) |
(2)用x表示出平衡时SO3、SO2和O2的浓度,代入K=
| c2(SO3) |
| c2(SO2)c(SO2) |
(3)根据常数的相对大小,判断平衡移动方向,再由温度对化学平衡影响判断.
解答:解:(1)2SO2 (g)+O2 (g)  2SO3(g)
2SO3(g)
开始 0.2mol/L 0.1mol/L 0mol/L
变化 0.18mol/L 0.09mol/L 0.18mol/L
平衡时 0.02mol/L 0.01mol/L 0.18mol/L
2分钟内,用O2表示该反应的平均反应速率为
=
=0.045mol?L-1?min-1
500℃时,该反应的平衡常数代入K=
=
=8.1×103(mol?L-1)-1
故答案为:0.045mol?L-1?min-1; 8.1×103(mol?L-1)-1
(2)2SO2 (g)+O2 (g) 2SO3(g)
2SO3(g)
开始 0.2mol/L 0.1mol/L 0mol/L
变化 0.2xmol/L 0.1xmol/L 0.2xmol/L
2分钟时 ( 0.2-0.2x)mol/L (0.1-0.1x)mol/L 0.2xmol/L
所以
=8.1×103
故答案为:
=8.1×103
(3)K=800(mol?L-1)-1小于8.1×103(mol?L-1)-1,平衡向逆反应方向移动,正反应为放热反应,则逆反应为吸热反应,升高温度向吸热方向进行,故温度高于500℃,
故答案为:>.
 2SO3(g)
2SO3(g)开始 0.2mol/L 0.1mol/L 0mol/L
变化 0.18mol/L 0.09mol/L 0.18mol/L
平衡时 0.02mol/L 0.01mol/L 0.18mol/L
2分钟内,用O2表示该反应的平均反应速率为
| △c(O2) |
| △t |
| 0.09mol/L |
| 2min |
500℃时,该反应的平衡常数代入K=
| c2 ( SO 3 ) |
| c2( SO 2)c( O 2) |
| (0.18mol/L)2 |
| (0.02mol/L)20.01mol/L |
故答案为:0.045mol?L-1?min-1; 8.1×103(mol?L-1)-1
(2)2SO2 (g)+O2 (g)
 2SO3(g)
2SO3(g)开始 0.2mol/L 0.1mol/L 0mol/L
变化 0.2xmol/L 0.1xmol/L 0.2xmol/L
2分钟时 ( 0.2-0.2x)mol/L (0.1-0.1x)mol/L 0.2xmol/L
所以
| (0.2x)2 |
| (0.2-0.2x)2(0.1-0.1x) |
故答案为:
| (0.2x)2 |
| (0.2-0.2x)2(0.1-0.1x) |
(3)K=800(mol?L-1)-1小于8.1×103(mol?L-1)-1,平衡向逆反应方向移动,正反应为放热反应,则逆反应为吸热反应,升高温度向吸热方向进行,故温度高于500℃,
故答案为:>.
点评:利用平衡常数的计算,进几年高考出现频率较高,平时学习要加以注意.

练习册系列答案
相关题目
已知2SO2(g)+O2(g)═2SO3(g),△H=-197.8kJ?mol-1,则反应:SO3 (g)═
O2 (g)+SO2 (g)的△H是( )
| 1 |
| 2 |
| A、+197.8kJ?mol-1 |
| B、+98.9kJ?mol-1 |
| C、-296.7kJ?mol-1 |
| D、-98.9kJ?mol-1 |
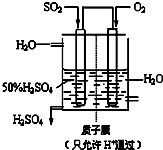
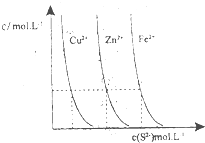 以下是对化学反应变化过程及结果的研究.按要求回答问题:
以下是对化学反应变化过程及结果的研究.按要求回答问题: