题目内容
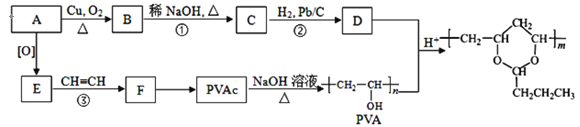
【题目】Cl2和H2O2是高中阶段最常见的两种氧化剂,经查阅资料Cl2氧化能力强于H2O2,能将H2O2氧化。为了验证该结论,学生设计了如下图所示的实验装置进行实验(夹持装置略去)。请回答下列问题。
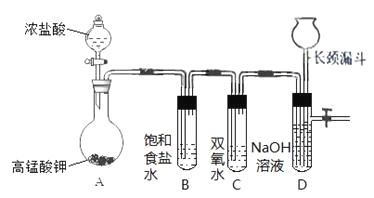
(1)A中的方程式为_____________________(用单线桥标电子转移方向与数目);
(2)试管B中饱和食盐水的作用__________________;
(3)试管C中加入5mL 30% 双氧水,发生反应的化学方程式____________________;
(4)试管D中充满10% NaOH溶液,NaOH溶液的作用是__________________;
(5)将浓盐酸注入圆底烧瓶A,当装置中的空气基本排尽后关闭止水夹,反应一段时间后试管D中的现象为_____________________________________________,试管D中的气体检验方法为____________;
(6)有的同学对上述实验中D试管中的气体来源产生质疑,你认为可能的来源有:_____________(用方程式回答)。对于质疑可以采用对比实验来解决。
【答案】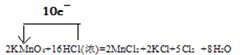 除去Cl2中混有的HCl Cl2+H2O2=2HCl+O2 吸收多余的Cl2 试管D中液面下降,长颈漏斗中液面上升; 打开止水夹,用带火星的木条检验,复燃,证明是氧气 2H2O2=2H2O+O2↑或Cl2+H2O=HCl+HclO,2HClO
除去Cl2中混有的HCl Cl2+H2O2=2HCl+O2 吸收多余的Cl2 试管D中液面下降,长颈漏斗中液面上升; 打开止水夹,用带火星的木条检验,复燃,证明是氧气 2H2O2=2H2O+O2↑或Cl2+H2O=HCl+HclO,2HClO![]() 2HCl+O2↑
2HCl+O2↑
【解析】
(1)高锰酸钾能够氧化浓盐酸制备氯气;
(2)浓盐酸易挥发,制备的氯气中含有氯化氢,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大;
(3)氯气与双氧水反应生成氯化氢和氧气;
(4)氯气有毒,直接排放会引起空气污染,氯气能够与氢氧化钠溶液反应,被吸收;
(5)氯气和过氧化氢反应生成氧气,氧气难溶于水,根据氧气具有助燃性进行验证氧气;
(6)过氧化化氢分解生成氧气,氯气和水反应生成盐酸和次氯酸,次氯酸分解生成氧气。
(1)高锰酸钾与浓盐酸反应生成氯化钾、氯化锰、氯气和水,方程式: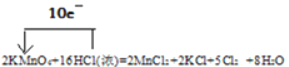 ;
;
(2)浓盐酸易挥发,制备的氯气中含有氯化氢,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,可以用饱和食盐水除去氯气中的氯化氢;
故答案为:除去Cl2中混有的HCl;
(3)氯气与双氧水反应生成氯化氢和氧气,化学方程式为:Cl2+H2O2=2HCl+O2,
故答案为:Cl2+H2O2=2HCl+O2;
(4)氯气有毒,直接排放会引起空气污染,氯气能够与氢氧化钠溶液反应,被氢氧化钠溶液吸收,所以可以用氢氧化钠吸收过量的氯气;
故答案为:吸收多余的氯气;
(5)Cl2+H2O2=2HCl+O2,当关闭止水夹,反应一段时间后试管D中因氧气不断增多,气体压强增大,所以试管D中液面下降,长颈漏斗中液面上升,氧气使带火星的木条复燃,可用此法验证氧气,
故答案为:试管D中液面下降,长颈漏斗中液面上升;该气体能使带火星的木条复燃,证明是氧气;
(6)试管D中气体来源可能为过氧化氢的分解2H2O2=2H2O+O2↑,也可能为氯气氯气和水反应生成盐酸和次氯酸,次氯酸分解,相应的化学方程式为:Cl2+H2O=HCl+HClO,2HClO![]() 2HCl+O2↑。
2HCl+O2↑。

 口算题天天练系列答案
口算题天天练系列答案【题目】 下表为元素周期表中第四周期的部分元素(从左到右按原子序数递增排列),根据要求回答下列问题:
K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge |
(1)以上元素的基态原子的电子排布中,4s轨道上只有1个电子的元素有______(填元素名称)。
(2)以上元素中,属于s区的元素有_____种,属于d区的元素有______种。
(3)第一电离能I1(Cr)________I1(Co)(填“>”、“<”或“=”,下同)。
(4)现有含钛的两种颜色的晶体,Ti3+的配位数均为6,一种为紫色,一种为绿色,相关实验证明,两种晶体的组成皆为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种配合物晶体的样品配成待测溶液;
b.分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的![]() 。试推断紫色晶体的化学式为_________。
。试推断紫色晶体的化学式为_________。
(5)含有元素K的盐的焰色反应为__________色。许多金属盐都可以发生焰色反应,其原因是____________。