题目内容
10.设NA代表阿伏加德罗常数,下列说法中,正确的是( )| A. | 2.3g金属钠全部变成钠离子时失去的电子数目为0.2NA | |
| B. | 2g氢气所含的原子数目为NA | |
| C. | 17gNH3所含的电子数为10NA | |
| D. | NA个氧分子和NA个氢分子的质量比等于16:1 |
分析 A、求出钠的物质的量,然后根据反应后变为+1价来分析;
B、氢气由氢原子构成;
C、求出氨气的物质的量,然后根据氨气为10电子分子;
D、等物质的量的物质的质量之比等于摩尔质量之比.
解答 解:A、2.3g钠的物质的量为0.1mol,而反应后变为+1价,故0.1mol钠失去0.1mol电子即0.1NA个,故A错误;
B、氢气由氢原子构成,故2g氢气中含有的氢原子的物质的量为n=$\frac{2g}{1g/mol}$=2mol,即2NA个,故B错误;
C、17g氨气的物质的量为1mol,而氨气为10电子分子,故1mol氨气中含10mol电子即10NA个,故C正确;
D、NA个氧分子和NA个氢分子的物质的量均为1mol,而等物质的量的物质的质量之比等于摩尔质量之比,故两者的质量之比为32:2=16:1,故D正确.
故选CD.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
20.金属镍有广泛的用途.粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,(已知:氧化性Fe2+<Ni2+<Cu2+),下列叙述正确的是( )
| A. | 阳极发生还原反应,其电极反应式:Ni2++2e-═Ni | |
| B. | 电解后,电解槽底部的阳极泥中只有Pt | |
| C. | 电解后,溶液中存在的阳离子只有Fe2+和Zn2+ | |
| D. | 电解过程中,阳极质量的减少与阴极质量的增加不相等 |
1.与3.2gSO2所含的氧原子数相等的CO2的质量为( )
| A. | 2.2g | B. | 4.4g | C. | 44g | D. | 22g |
18.下列化学用语不能正确表示相应粒子的是( )
| A. | C2H6的结构简式:CH3CH3 | B. | O2-的结构示意图: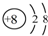 | ||
| C. | CO2的结构式:O=C=O | D. | HClO的电子式:H:Cl:O: |
5.下列说法正确的是( )
| A. | 标况下22.4 L H2O和 1 mol O2所含分子数相等 | |
| B. | 1 mol水中含有2 mol氢和1 mol氧 | |
| C. | 1 mol气态水比1 mol液态水所含的分子数多 | |
| D. | 3 mol O2 与2 mol H2O所含原子数相等 |
15.下列分子式只能表示一种物质的是( )
| A. | C3H4Cl2 | B. | CH4O | C. | C2H6O | D. | C2H4O2 |
2.下列有关离子浓度的比较正确的是( )
| A. | 0.1mol•L-1氨水中,c(OH-)<c(NH4+) | |
| B. | 10mL 0.02mol•L-1HCl溶液与10mL 0.02mol•L-1 Ba(OH)2溶液充分混合,c(Cl-)>c(Ba2+)>c(OH-)=c(H+) | |
| C. | 将0.1mol•L-1CH3COONa和0.1mol•L-1NH4Cl等体积混合后的溶液中,c(H+)+c(CH3COOH)>c(NH3•H2O)+c(OH-) | |
| D. | 0.1mol•L-1某二元弱酸碱性NaHA溶液中,c(H+)+c(H2A)═c(A2-)+c(OH-) |
19.吸食毒品危害身心、危害社会.其中对身心的危害描述,正确的有:( )
①中毒特征:嗜睡、感觉迟钝、运动失调、幻觉、妄想、定向障碍等.
②严重的身体戒断反应引起各种并发症,或由于痛苦难忍而自杀身亡.
③吸毒所致主要的精神障碍 是幻觉和思维障碍.他们的行为特点为吸毒而毁三观 碎节操.
④感染性疾病:静脉注射毒品给滥用者带来感染性合并症,最常见的有化脓性感染和乙形肝炎,及令人担忧 的艾滋病问题.
①中毒特征:嗜睡、感觉迟钝、运动失调、幻觉、妄想、定向障碍等.
②严重的身体戒断反应引起各种并发症,或由于痛苦难忍而自杀身亡.
③吸毒所致主要的精神障碍 是幻觉和思维障碍.他们的行为特点为吸毒而毁三观 碎节操.
④感染性疾病:静脉注射毒品给滥用者带来感染性合并症,最常见的有化脓性感染和乙形肝炎,及令人担忧 的艾滋病问题.
| A. | ① | B. | ①、② | C. | ①、②、③ | D. | ①、②、③、④ |
20.下列说法错误的是( )
| A. | 1 mol水 | B. | 0.3 mol硫酸 | C. | 0.5 mol钠 | D. | 1.5 mol氧 |