题目内容
镍具有优良的物理和化学特性,是许多领域尤其是高技术产业的重要原料。羰基法提纯粗镍涉及的两步反应依次为:
(1)Ni(S)+4CO(g) Ni(CO)4(g)+Q
Ni(CO)4(g)+Q
(2)Ni(CO)4(g)  Ni(S)+4CO(g)
Ni(S)+4CO(g)
完成下列填空:
(1)在温度不变的情况下,要提高反应(1)中Ni(CO4)的产率,可采取的措施有 、 。
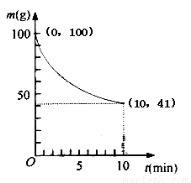
(2)已知在一定条件下的2L密闭容器中制备Ni(CO)4,粗镍(纯度98.5%,所含杂质不与CO反应)剩余质量和反应时间的关系如右图所示。Ni(CO)4在0~10min的平均反应速率为 。
(3)若反应(2)达到平衡后,保持其他条件不变,降低温度,重新达到平衡时 。
a.平衡常数K增大 b.CO的浓度减小
c.Ni的质量减小 d.v逆[Ni(CO)4]增大
(4)简述羰基法提纯粗镍的操作过程。
(1)及时移走Ni(CO)4,加压。
(2)0.05mol·L-min-。
(3)bc。
(4)先将粗镍和CO在50℃反应生成羰基镍,然后将羰基镍转移到另外一个中,升温至230℃热解得到纯镍。
解析(1)反应(1)是正向气体体积缩小的放热反应,因此根据平衡移动原理在温度不变的情况下采取可增大CO浓度,及时移走Ni(CO)4,加压的方法等提高产率;
(2)根据题意,反应的Ni为1 mol,则生成Ni(CO)4为1 mol,反应速率为1/(2×10)=0.05mol·L-min-;
(3)反应(2)是正向气体体积增大的吸热反应,则,降低温度平衡逆向移动,平衡常数K、CO的浓度、Ni的质量、v逆【Ni(CO)4】均减小;根据反应⑴⑵的特点可提纯粗镍。
【考点定位】 本题考查化学反应速率、平衡移动原理的应用。

练习册系列答案
相关题目
 镍具有优良的物理和化学特性,是许多领域尤其是高技术产业的重要原料.羰基法提纯粗镍涉及的两步反应依次为:
镍具有优良的物理和化学特性,是许多领域尤其是高技术产业的重要原料.羰基法提纯粗镍涉及的两步反应依次为:


 Ni(CO)4(g)+Q
Ni(CO)4(g)+Q Ni(S)+4CO(g)
Ni(S)+4CO(g)