题目内容
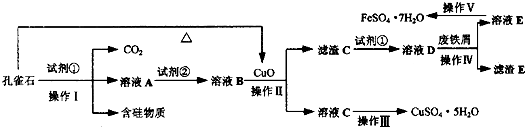
孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的氧化物,实验室以孔雀石为原料制备CuSO4·5H2O,步骤如下:

(1)写出Cu2(OH)2CO3在水中的沉淀溶解平衡方程式________,溶液A的金属离子有Cu2+、Fe2+、Fe3+.检验溶液A中Fe3+的最佳试剂为________,试剂①为________(从下列所给字母中选填,下同)
a.KMnO4
b.KI
c.H2O2
d.KSCN
(2)写出溶液A到溶液B的离子方程式________
(3)试剂②是CuO,还可以是下列的________,作用是________.
a.CuCl2
b.CuCO3
c.Cu(OH)2
d.CuSO4
(4)沉淀C的化学式为________.
答案:
解析:
解析:
|
(1)Cu2(OH)2CO3(s) (2)2Fe2++H2O2+2H+=2Fe2++2H2O(2分) (3)bc(2分) 消耗溶液中的H+调节pH,使Fe3+沉淀.(2分) (4)Fe(OH)3(1分) |

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目