题目内容
下列关于粒子的描述不正确的是( )
| A、H2O、NH3均是极性分子 | B、HS-和HCl均是含一个极性键的18电子粒子 | C、CO2和C2H2均为直线型分子 | D、D218O分子中所含中子、质子、电子的数目均相等 |
分析:A.分子中正负电荷中心不重合,从整个分子来看,电荷的分布是不均匀的,不对称的,这样的分子为极性分子,以极性键结合的双原子一定为极性分子,以极性键结合的多原子分子如结构对称,正负电荷的重心重合,电荷分布均匀,则为非极性分子;
B.HS-和HCl均是含18个电子,含有一个极性键;
C.CO2和C2H2的中心原子均为sp杂化空间构型为直线形;
D.1个D原子中含有一个质子、一个电子、一个中子,18O含有10个中子和8个质子.
B.HS-和HCl均是含18个电子,含有一个极性键;
C.CO2和C2H2的中心原子均为sp杂化空间构型为直线形;
D.1个D原子中含有一个质子、一个电子、一个中子,18O含有10个中子和8个质子.
解答:解:A.H2O中H、O元素形成的极性键,但结构不对称,属于极性分子;NH3中含有极性键,空间结构为三角锥形,正负电荷的中心不重合,属于极性分子,故A正确;
B.HS-和HCl都只含一个极性键,都具有18个电子,故B正确;
C.CO2和C2H2的中心原子均为含有2个价层电子对,为sp杂化,空间构型为直线形,故C正确;
D.1个D原子中含有一个质子、一个电子、一个中子,18O含有10个中子和8个质子,所以1 mol D218O中含质子、电子分别为10 NA,含有12NA中子,故D错误.
故选D.
B.HS-和HCl都只含一个极性键,都具有18个电子,故B正确;
C.CO2和C2H2的中心原子均为含有2个价层电子对,为sp杂化,空间构型为直线形,故C正确;
D.1个D原子中含有一个质子、一个电子、一个中子,18O含有10个中子和8个质子,所以1 mol D218O中含质子、电子分别为10 NA,含有12NA中子,故D错误.
故选D.
点评:本题考查极性分子和非极性分子、质子数、中子数、核外电子数及其相互联系,难度不大.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
关于下列粒子的描述不正确的是( )
A、PH3的电子式为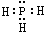 ,其热稳定性不如NH3 ,其热稳定性不如NH3 | B、HS-的电子式为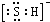 ,是含有极性键的18电子的粒子 ,是含有极性键的18电子的粒子 | C、CH2Cl2的电子式为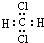 ,是分子结构呈四面体的分子 ,是分子结构呈四面体的分子 | D、KF的电子式为K+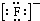 ,它是易溶于水的离子化合物 ,它是易溶于水的离子化合物 |