题目内容
在密闭容器中给CO和水蒸气的混合物加热到800℃时,有下列平衡:CO(g) +H2O(g)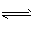 CO2(g)+ H2(g),且K=1,若用2mol CO和10mol H2O(g)相互混合并加热到800℃,则CO的转化率为
CO2(g)+ H2(g),且K=1,若用2mol CO和10mol H2O(g)相互混合并加热到800℃,则CO的转化率为
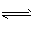 CO2(g)+ H2(g),且K=1,若用2mol CO和10mol H2O(g)相互混合并加热到800℃,则CO的转化率为
CO2(g)+ H2(g),且K=1,若用2mol CO和10mol H2O(g)相互混合并加热到800℃,则CO的转化率为 [ ]
A.16. 7%
B.50%
C.66. 7%
D.83. 5%
B.50%
C.66. 7%
D.83. 5%
D

练习册系列答案
相关题目
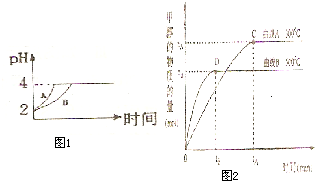 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题: