题目内容
下列离子在一定条件下能共存,且加入相应试剂后发生反应的离子方程式正确的是
| 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 | |
| A | Fe2+,N ,K+ ,K+ | 稀硫酸 | 3Fe2++N +4H+=3Fe3++NO↑+2H2O +4H+=3Fe3++NO↑+2H2O |
| B | Fe3+,I-,ClO- | 氢氧化钠溶液 | 3Fe3++3OH-=Fe(OH)3↓ |
| C | Ba2+,HC ,Cl- ,Cl- | 氢氧化钠溶液 | HC +OH-=C +OH-=C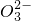 +H2O +H2O |
| D | Ag+,F-,N | 过量浓氨水 | Ag++OH-=AgOH↓ |
- A.A
- B.B
- C.C
- D.D
A
分析:A.该组离子能共存,加入稀硫酸,发生反应的离子方程式正确;
B.Fe3+与I-能发生氧化还原反应,I-与ClO-能发生氧化还原反应;
C.该组离子能共存,但加入氢氧化钠溶液生成的碳酸根离子和钡离子反应生成沉淀;
D.该组离子能共存,浓氨水为弱电解质,书写离子方程式应写化学式,加入过量浓氨水AgOH↓会溶解.
解答:A.Fe2+,NO3-,K+,均不反应能共存,加入稀硫酸发生反应3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,故A正确;
B.Fe3+与I-能发生氧化还原反应2Fe3++2I-=2Fe2++I2,则不能大量共存;I-与ClO-能发生氧化还原反应ClO-+2I-+2H2O=Cl-+I2+2OH-,则不能大量共存,加入氢氧化钠溶液发生反应的离子方程式3Fe3++3OH-=Fe(OH)3↓,故B错误;
C.Ba2+,HCO3-,Cl-,均不反应能共存,但加入氢氧化钠溶液生成的碳酸根离子和钡离子反应生成沉淀,发生反应的离子方程式为:Ba2++HCO3-+OH-=BaCO3↓+H2O,故C错误;
D.Ag+,F-,NO3-,均不反应能共存,但加入过量浓氨水,AgNO3+NH3?H2O=AgOH↓+NH4NO3,AgOH+2NH3?H2O=Ag(NH3)2OH+2H2O,总离子反应为Ag++3NH3?H2O=Ag(NH3)2++OH-+NH4++2H2O,故D错误;
故选A.
点评:本题考查离子共存及反应方程式问题,明确常见离子的性质及离子之间发生的反应是解答的关键,解答该题时注意各选项中的条件,题目难度中等.
分析:A.该组离子能共存,加入稀硫酸,发生反应的离子方程式正确;
B.Fe3+与I-能发生氧化还原反应,I-与ClO-能发生氧化还原反应;
C.该组离子能共存,但加入氢氧化钠溶液生成的碳酸根离子和钡离子反应生成沉淀;
D.该组离子能共存,浓氨水为弱电解质,书写离子方程式应写化学式,加入过量浓氨水AgOH↓会溶解.
解答:A.Fe2+,NO3-,K+,均不反应能共存,加入稀硫酸发生反应3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,故A正确;
B.Fe3+与I-能发生氧化还原反应2Fe3++2I-=2Fe2++I2,则不能大量共存;I-与ClO-能发生氧化还原反应ClO-+2I-+2H2O=Cl-+I2+2OH-,则不能大量共存,加入氢氧化钠溶液发生反应的离子方程式3Fe3++3OH-=Fe(OH)3↓,故B错误;
C.Ba2+,HCO3-,Cl-,均不反应能共存,但加入氢氧化钠溶液生成的碳酸根离子和钡离子反应生成沉淀,发生反应的离子方程式为:Ba2++HCO3-+OH-=BaCO3↓+H2O,故C错误;
D.Ag+,F-,NO3-,均不反应能共存,但加入过量浓氨水,AgNO3+NH3?H2O=AgOH↓+NH4NO3,AgOH+2NH3?H2O=Ag(NH3)2OH+2H2O,总离子反应为Ag++3NH3?H2O=Ag(NH3)2++OH-+NH4++2H2O,故D错误;
故选A.
点评:本题考查离子共存及反应方程式问题,明确常见离子的性质及离子之间发生的反应是解答的关键,解答该题时注意各选项中的条件,题目难度中等.

练习册系列答案
相关题目
已知下列分子或离子在一定条件下都可以氧化浓盐酸得到氯气,自身发生如下变化:
MnO4-→Mn2+Cr2O2-7→Cr3+ClO3-→Cl2 MnO2→Mn2+
如果分别用等物质的量的这些物质氧化足量的浓盐酸,得到Cl2最小的是( )
MnO4-→Mn2+Cr2O2-7→Cr3+ClO3-→Cl2 MnO2→Mn2+
如果分别用等物质的量的这些物质氧化足量的浓盐酸,得到Cl2最小的是( )
| A、MnO4- | B、Cr2O72- | C、CIO3- | D、MnO2 |
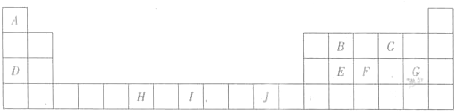
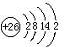
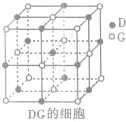 (3)H3+离子在一定条件下能形成结构复杂的配离子[HG(A2C)5]2+形成该配离子时,H3+离子接受了配体提供的
(3)H3+离子在一定条件下能形成结构复杂的配离子[HG(A2C)5]2+形成该配离子时,H3+离子接受了配体提供的