题目内容
某化学小组用稀硝酸与大理石的反应来探究影响化学反应速率的因素.所用硝酸浓度有1.00mol?L-1、2.00mol?L-1两种,大理石有细颗粒与粗颗粒两种规格,实验温度为25℃、35℃,每次实验硝酸溶液的体积均为2.50L、大理石用量均为150g.
(1)请完成以下实验设计表,并在实验目的一栏中填上对应的实验编号:
(2)实验①中CO2的物质的量随时间变化的关系见图:
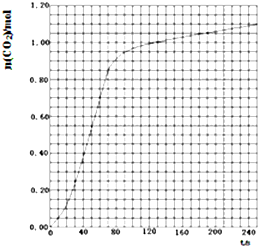
则在70-90s内以HNO3的浓度变化表示的化学反应速率(忽略溶液体积变化)为
(1)请完成以下实验设计表,并在实验目的一栏中填上对应的实验编号:
| 编号 | 温度 | 大理石规格 | HNO3浓度 /mol?L-1 |
实验目的 |
| ① | 25℃ | 粗颗粒 | 2.00 | (I)实验①和②探究硝酸浓度对该反应速率的影响; (II)实验①和 ③ ③ 探究温度对该反应速率的影响;(Ⅲ)实验①和 ④ ④ 探究大理石规格(粗、细)对该反应速率的影响. |
| ② | 25℃ | 粗颗粒 粗颗粒 |
1.00 1.00 | |
| ③ | 35℃ | 粗颗粒 粗颗粒 |
2.00 2.00 | |
| ④ | 25℃ | 细颗粒 细颗粒 |
2.00 2.00 |

则在70-90s内以HNO3的浓度变化表示的化学反应速率(忽略溶液体积变化)为
0.004mol?L-1?S-1
0.004mol?L-1?S-1
.分析:(1)根据实验的目的和影响化学反应速率的因素来设计实验;
(2)由CO2质量随时间变化的关系图得出70-90s二氧化碳的增加量,再根据方程式计算硝酸的量,然后计算实验①在70-90s范围内HNO3的平均反应速率.
(2)由CO2质量随时间变化的关系图得出70-90s二氧化碳的增加量,再根据方程式计算硝酸的量,然后计算实验①在70-90s范围内HNO3的平均反应速率.
解答:解:(1)由实验目的可知,探究浓度、温度、接触面积对化学反应速率的影响,
实验①和②探究硝酸浓度对该反应速率的影响,实验①②的温度、大理石规格相同,只有浓度不同;实验①③中只有温度不同,实验①④中只有大理石规格不同,故答案为:
(2)由图可知70至90S,CO2生成的物质的量为n(CO2)=0.95mol-0.85mol=0.1mol,
由CaCO3+2HNO3=Ca(NO3)2+CO2↑+H2O可知消耗HNO3的物质的量为n(HNO3)=0.1mol×2=0.2mol,
又溶液体积为2.5L,所以HNO3减少的浓度△c(HNO3)=
=0.08mol?L-1,
反应的时间t=90s-70s=20s,
所以HNO3在70-90S范围内的平均反应速率为v(HNO3)=
mol?L-1?S-1=0.004mol?L-1?S-1,
答:实验①在70-90s范围内HNO3的平均反应速率为0.004mol?L-1?S-1.
实验①和②探究硝酸浓度对该反应速率的影响,实验①②的温度、大理石规格相同,只有浓度不同;实验①③中只有温度不同,实验①④中只有大理石规格不同,故答案为:
| 编号 | 温度 | 大理石规格 | HNO3浓度 /mol?L-1 |
实验目的 |
| ① | (I)实验①和②探究硝酸浓度对该反应速率的影响; (II)实验①和?③探究温度对该反应速率的影响; (Ⅲ)实验①和④探究大理石规格(粗、细)对该反应速率的影响. | |||
| ② | 粗颗粒 | 1.00 | ||
| ③ | 粗颗粒 | 2.00 | ||
| ④ | 细颗粒 | 2.00 |
由CaCO3+2HNO3=Ca(NO3)2+CO2↑+H2O可知消耗HNO3的物质的量为n(HNO3)=0.1mol×2=0.2mol,
又溶液体积为2.5L,所以HNO3减少的浓度△c(HNO3)=
| 0.2mol |
| 2.5 |
反应的时间t=90s-70s=20s,
所以HNO3在70-90S范围内的平均反应速率为v(HNO3)=
| 0.08 |
| 20 |
答:实验①在70-90s范围内HNO3的平均反应速率为0.004mol?L-1?S-1.
点评:本题考查化学反应速率的影响因素及反应速率的计算,注意信息中提高的条件及图象的分析是解答的关键,较好的考查学生综合应用知识的能力.

练习册系列答案
相关题目

