题目内容
在一定温度下,把2体积N2和6体积H2通入一个带活塞的体积可变的容器中,活塞的一端与大气相通(如图所示),容器中发生以下反应,N2+3H2ƒ2NH3+Q,若反应达到平衡后,测得混合气体为7体积。据此回答下列问题:
(1)保持上述反应温度不变,设a、b、c分别代表初始加入的N2、H2和NH3的体积,如果反应平衡后混合气体中各物质的体积分数仍与上述平衡时完全相同。那么,若a=1,c=2,则b=________。在此情况下,反应起始时将向________方向进行(填“正”或“逆”)。若需规定起始时反应向逆方向进行,则c的范围是________(保持7体积)。
(2)在上述装置中,若需控制平衡后混合气体为6.5体积,则可采取的措施是________。其原因是________。

答案:
解析:
提示:
解析:
(1)3,正,1<c£4 (2)降温,见提示
|
提示:
提示:这是一个等效平衡原理的应用,在恒温恒压的条件下,a/b必须符合方程式的系数比。 N2 + 3H2=2NH3 起始 2 6 平衡 2-0.5 6-1.5 1[根据平衡时7体积] (1)a=1,c=2,则b=3,因为1+3+2<7,所以反应向正反应方向移动。因为原平衡c(NH3)=1,所以加入的氨气不能低于1,再根据等效平衡知识,推得c的范围为1<c£4。 (2)降低反应温度。因为6.5<7,向右移动,向放热反应方向移动。
|

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
 (2011?泰州二模)能源、材料和信息是现代社会的三大“支柱”.
(2011?泰州二模)能源、材料和信息是现代社会的三大“支柱”.
 (2012?唐山二模)【化学--选修物质结构与性质】
(2012?唐山二模)【化学--选修物质结构与性质】
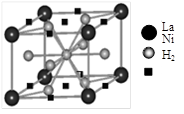
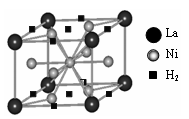
 水,由黄色变成鲜亮的红色,在空气中温度降低又变为黄色,具有可逆热色性;同时实验还表明它具有使激光倍频的二阶非线性光学性质。
水,由黄色变成鲜亮的红色,在空气中温度降低又变为黄色,具有可逆热色性;同时实验还表明它具有使激光倍频的二阶非线性光学性质。