题目内容
14.设NA为阿伏伽德罗常数的值,下列说法正确的是( )| A. | 0.5mol熔融的NaHSO4中含有的离子数目为1.5NA | |
| B. | 标准状况下,2.24LCl2溶于水,转移电子数为0.1NA | |
| C. | 氢气与氯气反应生成标准状况下22.4L氯化氢,则断裂化学键总数为NA | |
| D. | 电解精练铜时,转移1mol电子时,阳极溶解的铜的质量为32g |
分析 A.熔融硫酸氢钠电离出钠离子和硫酸氢根离子;
B.氯气溶于水是可逆反应,并不能完全反应;
C.当反应生成2molHCl时,断裂2mol化学键;
D.电解精炼铜的过程中,阳极溶解的不全都是铜.
解答 解:A.熔融的NaHSO4 只含Na+、HSO4-,0.5mol中含有离子为NA,故A错误;
B.氯气溶于水是可逆反应,并不能完全反应,2.24L标况下Cl2的物质的量为0.1mol,转移的电子数<0.1NA,故B错误;
C.生成标况下22.4LHCl气体,即1molHCl,消耗H2和Cl2各0.5mol,断裂化学键各0.5mol,断键总数NA,故C正确;
D.电解精炼铜,阳极为粗铜,其中还含有杂质,当转移1mol电子时,溶解的铜质量小于32g,故D错误.
故选C.
点评 本题考查阿伏伽德罗常数的计算,注意可逆反应的不完全性,气体摩尔体积22.4L/mol使用的条件等细节问题,题目难度不大.

练习册系列答案
相关题目
4.下列说法错误的是( )
| A. | 淀粉、纤维素、蛋白质是天然有机高分子化合物 | |
| B. | 糖类物质的组成元素是C、H、O三种 | |
| C. | 油脂是混合物,没有固定的熔点 | |
| D. | 淀粉和纤维素互为同分异构体 |
5.下列说法正确的是( )
| A. | NaCl的摩尔质量是58.5 g/mol | |
| B. | 18gH2O中所含水分子的物质的量是0.5mol | |
| C. | 22gCO2中所含原子数约为3×6.02×1023 | |
| D. | 任何条件下,22.4 L氢气中所含氢分子数都约为6.02×1023 |
2.设NA代表阿伏加德罗常数的值,下列叙述不正确的是( )
| A. | 20gD2O含电子数目为10NA | |
| B. | 标准状态下84gC3H6中含碳碳双键的数目为2NA | |
| C. | 1 L 0.1 mol/L NH4NO3溶液中含铵根离子数目小于0.1NA | |
| D. | 标准状态下44.8LCl2与足量水反应转移的电子数目一定小于2NA |
9.有一系列有机物分子,每个碳原子与周围3个碳原子形成碳碳单键,碳原子剩余价键被氢原子饱和.其中甲、乙、丙三种有机物结构如图所示,下列关于它们的描述正确的是( )

| A. | 甲、乙、丙组成结构相似,互为同系物 | |
| B. | 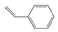 是丙的同分异构体 是丙的同分异构体 | |
| C. | 乙的二氯代物有4种 | |
| D. | 甲、乙、丙均为不饱和烃,它们都能使溴的CCl4溶液褪色 |
19.下列不能说明氯的非金属性比硫强的事实是( )
①HCl比H2S稳定
②HCl和H2S的水溶液前者的酸性强
③HClO4酸性比H2SO4强
④Cl2能与H2S反应生成S
⑤Cl原子能得1个电子变成稳定离子而S原子能得两个电子
⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS.
①HCl比H2S稳定
②HCl和H2S的水溶液前者的酸性强
③HClO4酸性比H2SO4强
④Cl2能与H2S反应生成S
⑤Cl原子能得1个电子变成稳定离子而S原子能得两个电子
⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS.
| A. | ②⑤ | B. | ①② | C. | ①②⑤ | D. | ①③⑤ |
1.不同温度下BaCO3在水中的沉淀溶解平衡曲线如图所示(已知T1<T2<T3),下列说法正确的是( )
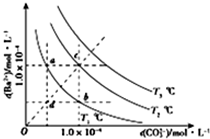

| A. | T2温度下将d点的溶液蒸发浓缩可变为c点 | |
| B. | a点的Ksp小于B点的Ksp | |
| C. | b点溶液中加入BaCl2固体可变为c点 | |
| D. | a点溶液蒸发浓缩恢复到原温度可变为b点 |
18.下列对乙烯和和聚乙烯的描述中,不正确的是( )
| A. | 乙烯是纯净物,聚乙烯是混合物,都能使酸性KMnO4溶液褪色 | |
| B. | 取等质量的乙烯和和聚乙烯完全燃烧后,生成的CO2和H2O的质量分别相等 | |
| C. | 常温下乙烯为气态,聚乙烯为固态 | |
| D. | 乙烯可以发生加成聚合反应生成聚乙烯,聚乙烯的单体是乙烯 |
19.下列说法中,正确的是( )
| A. | SO2能使酸性KMnO4溶液褪色,说明SO2具有还原性 | |
| B. | SO2能使品红溶液褪色,其漂白原理与氯水相同 | |
| C. | SO2是酸性氧化物,可以用澄清石灰水来鉴别SO2与CO2 | |
| D. | 用水吸收硫在过量氧气中燃烧的产物,可用于工业制备硫酸 |