题目内容
14.ag氯气与bg氢气混合点燃爆炸,试讨论a、b满足什么条件时:(1)恰好完全反应;
(2)氯气过量,并分别计算出生成氯化氢各多少克?
分析 发生H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl,由反应可知,物质的量相等时恰好完全反应,氯气过量时氢气完全反应,结合n=$\frac{m}{M}$及反应计算.
解答 解:发生H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl,
(1)物质的量相等时恰好完全反应,则$\frac{ag}{36.5g/mol}$=$\frac{bg}{2g/mol}$,即2a=36.5b,
答:2a=36.5b时恰好完全反应;
(2)氯气过量,$\frac{ag}{36.5g/mol}$>$\frac{bg}{2g/mol}$,即2a>36.5b,氢气完全反应,由H原子守恒可知,生成HCl为$\frac{bg}{2g/mol}$×2×36.5g/mol=36.5bg,
答:满足条件为2a>36.5b,生成HCl为36.5bg.
点评 本题考查化学反应方程式的计算,为高频考点,把握发生的反应及过量判断为解答的关键,侧重分析与计算能力的考查,注意量少的物质完全反应,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.下列说法不正确的是( )
| A. | ${\;}_{2}^{3}$He的中子数是2 | B. | 白磷、红磷互为同素异形体 | ||
| C. | 18O和16O是互为同位素 | D. | 正丁烷和异丁烷互为同分异构体 |
2.某有机物的结构简式如图所示.下列有关该物质的说法正确的是( )
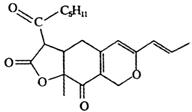

| A. | 该物质的分子式为C21H25O5 | |
| B. | 该物质含有四种含氧官能团 | |
| C. | 1 mol该物质在一定条件下最多可以和5mol H2反应 | |
| D. | 1 mol该物质最多能与2 mol NaOH反应 |
9.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 18gH2O含有10NA个质子 | |
| B. | 2L0.5mol•L-1硫酸钾溶液中阴离子所带电荷数为NA | |
| C. | 标准状况下,22.4L氨水含有NA个NH3分子 | |
| D. | 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.25NA |
19.NA表示阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 1mol12C原子的质量是12g,1个12C原子的质量是$\frac{12}{{N}_{A}}$g | |
| B. | 在常温常压下,11.2L N2含有分子数为0.5NA | |
| C. | 18 g水所含有的氢原子数目为2NA,氧原子数目为NA | |
| D. | 1L 0.1mol•L-1 Na2SO4溶液中,Na+和SO${\;}_{4}^{2-}$的离子总数是0.3NA |
6.下列离子在溶液中因发生氧化还原反应而不能大量共存的是( )
| A. | H+、Na+、HCO3-、SO42- | B. | Ba2+、NO3-、SO42-、K+ | ||
| C. | H+、NO3-、Fe2+、Na+ | D. | Mg2+、Fe3+、Cl-、OH- |
12.下列气体主要成分不是甲烷的是( )
| A. | 天然气 | B. | 沼气 | C. | 煤矿坑道气 | D. | 液化石油气 |