题目内容
某1.2mol?L-1 Fe2 (SO4)3和2.4mol?L-1 CuSO4的混合溶液100mL,最多能溶解铁粉的物质的量为( )
| A、0.30mol | B、0.36mol | C、0.48mol | D、0.56mol |
分析:因氧化性Fe3+>Cu2+,则加入铁粉,先发生Fe+Fe2 (SO4)3=3FeSO4,后发生Fe+CuSO4=FeSO4+Cu,结合化学反应方程式即可计算.
解答:解:n(Fe2 (SO4)3)=1.2mol/L×0.1L=0.12mol,n(CuSO4)=2.4mol/L×0.1L=0.24mol,
先后发生Fe+Fe2(SO4)3=3FeSO4、Fe+CuSO4=FeSO4+Cu,
由方程式可知消耗Fe的物质的量为n(Fe)=n(Fe2 (SO4)3)+n(CuSO4)=0.12mol+0.24mol=0.36mol,
故选B.
先后发生Fe+Fe2(SO4)3=3FeSO4、Fe+CuSO4=FeSO4+Cu,
由方程式可知消耗Fe的物质的量为n(Fe)=n(Fe2 (SO4)3)+n(CuSO4)=0.12mol+0.24mol=0.36mol,
故选B.
点评:本题以铁的性质为载体考查化学方程式的计算,侧重于学生的分析能力和计算能力的考查,为高频考点,注意相关方程式的书写和计算公式的运算.

练习册系列答案
相关题目
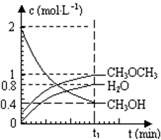 已知二甲醚是一种重要的清洁燃料,可以通过CH3OH分子间脱水制得:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=23.5kJ?mol-1.在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示.请回答下列问题:
已知二甲醚是一种重要的清洁燃料,可以通过CH3OH分子间脱水制得:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=23.5kJ?mol-1.在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示.请回答下列问题: