题目内容
过二硫酸钾(K2S2O8)在高于
完成下列问题:
(1)试从图中选取几种必要的装置,连接成一整套实验装置,这些被选用装置的接口编号连接顺序为______________________________________________。
(2)观察到的三氧化硫的颜色和状态是___________,将三氧化硫与水反应,鉴定反应产物中阴离子的方法是___________________________。
(3)若实验时称取过二硫酸钾的质量为W g,测得氧气的体积(折算成标准状况)为a mL,则此过二硫酸钾的纯度为_________________。
(1)IGHFEJ(G、H的顺序可以颠倒)
(2)无色晶体 加入稀盐酸,无明显现象,再加BaCl2溶液,有白色沉淀生成 (3)![]() %
%
解析:此实验的原理是通过测定产物O2的体积,来确定反应物K2S2O8的纯度。因为是固体加热分解制取气体,所以选用装置Ⅴ;要测定O2的体积,需先用冰水冷却,将气体产物中的SO3分离出来,这样由G端(或H端)出来的气体产物仅是O2;由于是利用测量排出水的体积的方法来测定O2的体积,所以应选用装满水的集气瓶Ⅲ,为了将水压出来,气体必须从F端进入,使水从E端排出,用量筒Ⅵ收集并测量其体积。得到的SO3是无色晶体,它与水反应生成H2SO4,反应产物的阴离子是![]() ,可以用BaCl2溶液来鉴定;从题目中给出的化学反应方程式可知,2 mol K2S2O8分解产生1 mol O2,所以K2S2O8的纯度为
,可以用BaCl2溶液来鉴定;从题目中给出的化学反应方程式可知,2 mol K2S2O8分解产生1 mol O2,所以K2S2O8的纯度为![]() %。
%。

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
硫元素的含氧酸盐在工业上用途广泛.
(1)工业上用Na2SO3溶液处理工业尾气中的SO2,表中数据表示反应过程中
随pH变化的关系:
简述
=1时,溶液pH=7.2的原因: ;若用0.20mol/L的NaOH溶液(反应前后溶液体积不变)吸收SO2,若反应后溶液呈中性,则c(HSO3-)+2c(SO32-)= mol/L.
(2)已知Ki1(H2SO3)>Ki(HAc)>Ki2(H2SO3)>Ki2(H2CO3),要使NaHSO3溶液中c(Na+):c(HSO3-)接近1:1,可在溶液中加入少量 .
a.H2SO3溶液 b.NaOH溶液 c.冰醋酸 d.Na2CO3
(3)实验室通过低温电解KHSO4溶液制备过二硫酸钾K2S2O8,写出熔融KHSO4的电离方程式: .
(4)S2O82-有强氧化性,还原产物为SO42-,硫酸锰(MnSO4)和过硫酸钾(K2S2O8)两种盐溶液在银离子催化下可发生反应,得到紫红色溶液.书写此反应的化学方程式: .
(5)已知:S2O32-有较强的还原性,实验室可用I-测定K2S2O8样品的纯度:反应方程式为:
S2O82-+2I-→2SO42-+I2 …①;
I2+2S2O32-→2I-+S4O62-…②.
则S2O82-、S4O62-、I2氧化性强弱顺序: .
(6)K2S2O8是偏氟乙烯(CH2=CF2)聚合的引发剂,偏氟乙烯由CH3-CClF2气体脱去HCl制得,生成0.5mol偏氟乙烯气体要吸收54kJ的热,写出反应的热化学方程式 .
(1)工业上用Na2SO3溶液处理工业尾气中的SO2,表中数据表示反应过程中
| n(SO32-) |
| n(HSO3-) |
|
91:9 | 1:1 | 9:91 | ||
| 室温下pH | 8.2 | 7.2 | 6.2 |
| n(SO32-) |
| n(HSO3-) |
(2)已知Ki1(H2SO3)>Ki(HAc)>Ki2(H2SO3)>Ki2(H2CO3),要使NaHSO3溶液中c(Na+):c(HSO3-)接近1:1,可在溶液中加入少量
a.H2SO3溶液 b.NaOH溶液 c.冰醋酸 d.Na2CO3
(3)实验室通过低温电解KHSO4溶液制备过二硫酸钾K2S2O8,写出熔融KHSO4的电离方程式:
(4)S2O82-有强氧化性,还原产物为SO42-,硫酸锰(MnSO4)和过硫酸钾(K2S2O8)两种盐溶液在银离子催化下可发生反应,得到紫红色溶液.书写此反应的化学方程式:
(5)已知:S2O32-有较强的还原性,实验室可用I-测定K2S2O8样品的纯度:反应方程式为:
S2O82-+2I-→2SO42-+I2 …①;
I2+2S2O32-→2I-+S4O62-…②.
则S2O82-、S4O62-、I2氧化性强弱顺序:
(6)K2S2O8是偏氟乙烯(CH2=CF2)聚合的引发剂,偏氟乙烯由CH3-CClF2气体脱去HCl制得,生成0.5mol偏氟乙烯气体要吸收54kJ的热,写出反应的热化学方程式
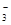 +4H++3e-→NO+2H2O
+4H++3e-→NO+2H2O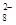 +2I-=2SO
+2I-=2SO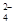 +I2
+I2 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2 +8H2O若生成11.2LNO(标准状况),则反应中转移电子的物质的量为__________。
+8H2O若生成11.2LNO(标准状况),则反应中转移电子的物质的量为__________。 2SO42-+I2通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe2+对上述反应的催化过程:____________________________、______________________________。
2SO42-+I2通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe2+对上述反应的催化过程:____________________________、______________________________。