题目内容
保护环境已成为全球性的重大课题之一.下列各项中,属于因人类生产、生活对环境造成破坏而带来的后果的是( )
①土地沙漠化 ②酸雨 ③水资源危机 ④南极上空臭氧空洞变大 ⑤沙尘暴.
①土地沙漠化 ②酸雨 ③水资源危机 ④南极上空臭氧空洞变大 ⑤沙尘暴.
分析:根据士地沙漠化、水资源危机、酸雨、南极上空臭氧空洞变大、沙尘暴形成的原因分析本题.
解答:解:①士地沙漠化是由于人类的乱砍滥伐造成的;
②酸雨主要是人类使用含硫元素的物质燃烧后生成二氧化硫造成的;
③水资源危机由于人类对水体的污染和浪费水造成的;
④南极上空臭氧空洞变大由于人类使用含氟冰箱等造成的;
⑤沙尘暴形成的原因主要是植物的大量砍伐造成的.
则①②③④⑤都属于因人类生产、生活对环境造成破坏而带来的后果.
故选D.
②酸雨主要是人类使用含硫元素的物质燃烧后生成二氧化硫造成的;
③水资源危机由于人类对水体的污染和浪费水造成的;
④南极上空臭氧空洞变大由于人类使用含氟冰箱等造成的;
⑤沙尘暴形成的原因主要是植物的大量砍伐造成的.
则①②③④⑤都属于因人类生产、生活对环境造成破坏而带来的后果.
故选D.
点评:本题考查常见环境污染及治理,题目难度不大,注意人类生产、生活对环境各个方面造成严重的影响,我们应该关注与人类生存环境关系密切的环境问题.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
(Ⅰ)保护环境已成为当前和未来的一项全球性重大课题.为解决目前燃料使用过程中的环境污染问题,并缓解能源危机,有的专家提出利用太阳能促使燃料循环使用的构想,如图1所示:
请回答下列问题:
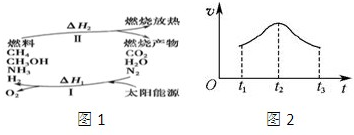
(1)过程Ⅰ的能量转化形式为 能转化为 能.
(2)上述转化过程中,△H1和△H2的关系是 .
(3)断裂1mol化学键所需的能量见下表:
常温下,N2与H2O反应生成NH3的热化学方程式为 .
(Ⅱ)在一试管中加入0.01mol/L的KMnO4酸性溶液和0.1mol/L H2C2O4溶液,在恒温下发生如下反应:
2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2+8H2O;5分钟后测得Mn2+的浓度为0.004mol/L;
(4)试计算0-5分钟内,v(H2C2O4)= ;
(5)如果反应从开始进行一段时间后,速率-时间图象如图2:试解释t1-t2,t2-t3速率变化的原因. .
请回答下列问题:

(1)过程Ⅰ的能量转化形式为
(2)上述转化过程中,△H1和△H2的关系是
(3)断裂1mol化学键所需的能量见下表:
| 共价键 | H-N | H-O | N≡N | O═O |
| 断裂1mol化学键所需能量/(kJ?mol-1) | 393 | 460 | 941 | 499 |
(Ⅱ)在一试管中加入0.01mol/L的KMnO4酸性溶液和0.1mol/L H2C2O4溶液,在恒温下发生如下反应:
2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2+8H2O;5分钟后测得Mn2+的浓度为0.004mol/L;
(4)试计算0-5分钟内,v(H2C2O4)=
(5)如果反应从开始进行一段时间后,速率-时间图象如图2:试解释t1-t2,t2-t3速率变化的原因.