��Ŀ����
����Ŀ��Ϊ�˲ⶨij�л���A�Ľṹ��������ʵ�飺 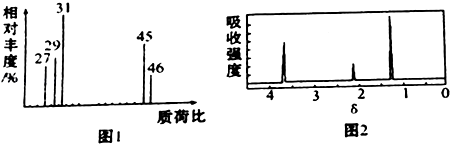
�ٽ�4.6g���л�����ȫȼ�գ�����0.2mol CO2��5.4gH2O��
���������Dzⶨ����Է�������������ͼ1��ʾ������ͼ��
���ú˴Ź����Ǵ����û�����õ���ͼ2��ʾͼ�ף�ͼ������������֮����1��2��3
������������⣺
��1���л���A����Է��������� ��
��2���л���A��ʵ��ʽ�� ��
��3���ܷ����A��ʵ��ʽȷ��A�ķ���ʽ����ܡ����ܡ��������ܣ���A�ķ���ʽ���������ܣ���˿ղ����
��4��д���л���A���ܵĽṹ��ʽ ��
���𰸡�
��1��46
��2��C2H6O
��3���ܣ�C2H6O
��4��CH3CH2OH
���������⣺��1����A������ͼ�У�����ʺɱ�Ϊ46����������Է�������Ҳ��46�����Դ��ǣ�46��
��2.��4.6 g���л����У�n��C��=n��CO2��=0.2 mol�����е�̼ԭ�ӵ�����Ϊm��C��=0.2 mol��12 gmol��1=2.4 g����ԭ�ӵ����ʵ���Ϊ��n��H��= ![]() ��2=0.6 mol����ԭ�ӵ�����Ϊm��H��=0.6 mol��1 gmol��1=0.6 g�����л�����m��O��=4.6g��2.4 g��0.6g=1.6g����Ԫ�ص����ʵ���Ϊn��O��=
��2=0.6 mol����ԭ�ӵ�����Ϊm��H��=0.6 mol��1 gmol��1=0.6 g�����л�����m��O��=4.6g��2.4 g��0.6g=1.6g����Ԫ�ص����ʵ���Ϊn��O��= ![]() =0.1 mol����n��C����n��H����n��O��=0.2 mol��0.6 mol��0.1 mol=2��6��1������A��ʵ��ʽ��C2H6O�����Դ��ǣ�C2H6O��
=0.1 mol����n��C����n��H����n��O��=0.2 mol��0.6 mol��0.1 mol=2��6��1������A��ʵ��ʽ��C2H6O�����Դ��ǣ�C2H6O��
��3.�����л�������ʽΪC2H6O��Hԭ���Ѿ�����Cԭ�ӵ��ļ۽ṹ�����ʽ��Ϊ����ʽ�����Դ��ǣ��ܣ�C2H6O��
��4.��A���������ֿ��ܵĽṹ��CH3OCH3��CH3CH2OH����Ϊǰ�ߣ����ں˴Ź���������Ӧֻ��1���壻��Ϊ���ߣ����ں˴Ź���������Ӧ��3���壬����3��������֮����1��2��3����ȻCH3CH2OH�������⣬����AΪ�Ҵ���
���Դ��ǣ�CH3CH2OH��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ���������ֿ���������A��B��C������A��B���Σ�C�Ǽ��������ˮ���������������������±���ʾ��
������ | Na+ H+ Ba2+ |
������ | OH�� CO32�� SO42�� |
��������������ش����⣺
��1��C�Ļ�ѧʽΪ ��
��2��A��Һ��B��Һ��Ӧ����������X����X�Ļ�ѧʽΪ �� �÷�Ӧ�����ӷ���ʽΪ ��
��3��A��B��Һ��C��Һ��Ӧ�ɷֱ����ɰ�ɫ����D��E������D������ϡ���ᣮ
��B�Ļ�ѧʽΪ �� ������Һ��B�������ӵ��Լ�Ϊ ��
��D����ϡ��������ӷ���ʽΪ
��D��E�Ļ����a g�������������ᣬ��ȫ��Ӧ���ɵ������ڱ�״�������ΪVL��������E�ڻ�����е����������ı���ʽΪ ��