题目内容
味精的主要成分是谷氨酸一钠盐( ),可用淀粉发酵法生产.
),可用淀粉发酵法生产.(1)发酵法第一步是使淀粉水解.实验室中淀粉在酸性条件下水解为单糖的化学方程式是______
【答案】分析:(1)淀粉在酸作用下水解生成葡萄糖方程式;淀粉水解得到单糖葡萄糖分子结构中含有醛基,利用醛基的检验方法选择试剂为新制银氨溶液,或新制氢氧化铜悬浊液;
(2)加入甲醛隐藏氨基避免干扰羧基和碱的反应
(3)①依据氯离子守恒及反应过程硝酸银的物质的量可以计算得到该味精样品中NaCl的质量分数;
②根据氯化银的溶解平衡运用平衡移动原理进行解释.
解答:解:(1)淀粉在酸作用下水解生成葡萄糖,水解方程式为:(C6H10O5)n+nH2O nC6H12O6 ;
nC6H12O6 ;
a、NaOH溶液、氨水、AgNO3溶液,氢氧化钠中和淀粉水解需要的催化剂,氨水、AgNO3溶液可以制备银氨溶液遇到醛基加热反应出现银镜反应,故A正确;
b、H2SO4溶液、碘水,只能检验是否存在淀粉,但是无法检验淀粉水解生成了葡萄糖,故b错误;
c、NaOH溶液、CuSO4溶液,氢氧化钠中和淀粉水解需要的催化剂,NaOH溶液、CuSO4溶液 可以制备氢氧化铜浊液和单糖加热反应生成砖红色沉淀,故c正确;
d、H2SO4溶液、CuSO4溶液,不能中和淀粉水解需要的酸催化剂,不能检验醛基的存在,故d错误;
故答案为:(C6H10O5)n+nH2O nC6H12O6 ; a、c;
nC6H12O6 ; a、c;
(2)依据反应R-NH2+HCHO→R-N=CH2+H2O,加入甲醛和氨基结合保护,避免影响氢氧化钠中和羧基的反应,
故答案为:避免显碱性的氨基影响羧基和NaOH的中和反应;
(3)①已知:AgSCN是难溶于水的沉淀,设测定过程中所消耗的AgNO3溶液和NH4SCN溶液的体积分别为V1mL和V2mL,硝酸银沉淀氯离子,过量的硝酸银被NH4SCN溶液沉淀生成AgSCN沉淀,依据氯元素守恒得到氯化钠质量分数: ×100%=
×100%= ,
,
故答案为: ;
;
②由于AgCl在溶液中存在平衡:AgCl(s)?Ag+(aq)+Cl-(aq),加入NH4SCN溶液后,SCN-与Ag+结合生成更难溶的AgSCN沉淀,使AgCl的溶解平衡向右移动,NH4SCN消耗量增大,导致测定结果低于实际值,
故答案为:AgCl在溶液中存在平衡:AgCl(s)?Ag+(aq)+Cl-(aq),加入NH4SCN溶液后,SCN-与Ag+结合生成更难溶的AgSCN沉淀,使AgCl的溶解平衡向右移动,NH4SCN消耗量增大.
点评:本题考查了物质性质的实验探究,物质组成的分析判断,实验基本操作和实验过程的分析应用时解题关键,题目难度中等
(2)加入甲醛隐藏氨基避免干扰羧基和碱的反应
(3)①依据氯离子守恒及反应过程硝酸银的物质的量可以计算得到该味精样品中NaCl的质量分数;
②根据氯化银的溶解平衡运用平衡移动原理进行解释.
解答:解:(1)淀粉在酸作用下水解生成葡萄糖,水解方程式为:(C6H10O5)n+nH2O
 nC6H12O6 ;
nC6H12O6 ;a、NaOH溶液、氨水、AgNO3溶液,氢氧化钠中和淀粉水解需要的催化剂,氨水、AgNO3溶液可以制备银氨溶液遇到醛基加热反应出现银镜反应,故A正确;
b、H2SO4溶液、碘水,只能检验是否存在淀粉,但是无法检验淀粉水解生成了葡萄糖,故b错误;
c、NaOH溶液、CuSO4溶液,氢氧化钠中和淀粉水解需要的催化剂,NaOH溶液、CuSO4溶液 可以制备氢氧化铜浊液和单糖加热反应生成砖红色沉淀,故c正确;
d、H2SO4溶液、CuSO4溶液,不能中和淀粉水解需要的酸催化剂,不能检验醛基的存在,故d错误;
故答案为:(C6H10O5)n+nH2O
 nC6H12O6 ; a、c;
nC6H12O6 ; a、c;(2)依据反应R-NH2+HCHO→R-N=CH2+H2O,加入甲醛和氨基结合保护,避免影响氢氧化钠中和羧基的反应,
故答案为:避免显碱性的氨基影响羧基和NaOH的中和反应;
(3)①已知:AgSCN是难溶于水的沉淀,设测定过程中所消耗的AgNO3溶液和NH4SCN溶液的体积分别为V1mL和V2mL,硝酸银沉淀氯离子,过量的硝酸银被NH4SCN溶液沉淀生成AgSCN沉淀,依据氯元素守恒得到氯化钠质量分数:
 ×100%=
×100%= ,
,故答案为:
 ;
;②由于AgCl在溶液中存在平衡:AgCl(s)?Ag+(aq)+Cl-(aq),加入NH4SCN溶液后,SCN-与Ag+结合生成更难溶的AgSCN沉淀,使AgCl的溶解平衡向右移动,NH4SCN消耗量增大,导致测定结果低于实际值,
故答案为:AgCl在溶液中存在平衡:AgCl(s)?Ag+(aq)+Cl-(aq),加入NH4SCN溶液后,SCN-与Ag+结合生成更难溶的AgSCN沉淀,使AgCl的溶解平衡向右移动,NH4SCN消耗量增大.
点评:本题考查了物质性质的实验探究,物质组成的分析判断,实验基本操作和实验过程的分析应用时解题关键,题目难度中等

练习册系列答案
相关题目
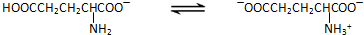
 ),可用淀粉发酵法生产.
),可用淀粉发酵法生产.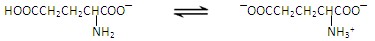
 ),可用淀粉发酵法生产.
),可用淀粉发酵法生产.