题目内容
3.以下能正确表示电离方程式的是( )| A. | BaSO4(s)?Ba2+(aq)+SO42- (aq) | B. | HClO═H++ClO- | ||
| C. | NaHSO4?Na++H++SO42- | D. | H2S?H++HS-、HS-?H++S2- |
分析 化学式和离子符号表示电离过程的式子,称为电离方程式,表示物质溶解于水时电离成离子的化学方程式,离子所带电荷数一般可根据它们在化合物中的化合价来判断,所有阳离子带的正电荷总数与所有阴离子所带的负电荷总数相等,离子团不能拆开.强电解质用等号,弱电解质用可逆号,据此分析.
解答 解:A.BaSO4是强电解质,能完全电离,电离方程式用等号,电离方程式为:BaSO4=Ba2++SO42-,故A错误;
B.HClO是弱酸,不能完全电离,用可逆号,正确的电离方程式为:HClO?H++ClO-,故B错误;
C.NaHSO4是强电解质,NaHSO4在水中电离出钠离子和硫酸根离子和氢离子,电离方程式为:NaHSO4═Na++H++SO42-,故C错误;
D.H2S是二元弱酸,在溶液中的电离分步进行,电离方程式为:H2S?H++HS-、HS-?H++S2-,故D正确.
故选D.
点评 本题难度不大,书写电离方程式时注意离子的正确书写、电荷守恒、离子团不能拆开,注意多元弱酸分步电离,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.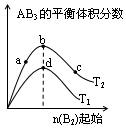 某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是( )
某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是( )
 某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是( )
某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是( )| A. | 图中T2一定大于T1 | |
| B. | 图中b点速率一定大于d点速率 | |
| C. | 达到平衡时,A2的转化率大小为:c>b>a | |
| D. | 加入催化剂可以使状态d变为状态b |
11.如图所示的各种尾气吸收装置中,适合于吸收HCl气体,而且能防止倒吸的有( )

| A. | ①②④⑤ | B. | ②③④⑤ | C. | ②④⑤ | D. | ③④ |
18.下列反应的离子方程式书写正确的是( )
| A. | 碳酸钙与盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| B. | 稀H2SO4与铁粉反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| D. | 将氢氧化铁放入盐酸中:Fe(OH)3+3H+═Fe3++3H2O |
8.实验室为了妥善保存硫酸亚铁溶液,常加入少量的( )
| A. | 铁粉 | B. | 铜粉 | C. | 锌粉 | D. | Fe2(SO4)3 |
15.下列各组物质各自形成的晶体,均属于分子晶体的化合物是( )
| A. | NH3、HD、CH4 | B. | HCl、CO2、H2SO4 | C. | SO2、SiO2、P2O5 | D. | CCl4、Na2S、H2O |
13.在实验室完成下列实验时,不需要考虑尾气处理的是( )
| A. | Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O | B. | Cu+2H2SO4(浓)$\frac{\underline{\;△\;}}{\;}$CuSO4+SO2↑+2H2O | ||
| C. | 3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O | D. | 2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑ |