题目内容
14.用单线桥表示下列反应方程式电子转移的方向和数目:(1)2H2S+SO2═3S+2H2O
(2)2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑
氧化产物:还原产物=3:2
(3)2FeCl2+Cl2═2FeCl3
(4)8NH3+3Cl2═N2+6NH4Cl
被氧化的氨气:参加反应的氨气=1:4.
分析 (1)反应2H2S+SO2═3S↓+2H2O中硫元素的化合价变化为:由+4价、-2价分别变为0价,该反应中氧化产物和还原产物都是硫单质;
(2)反应中Cl元素化合价由+5价降低为KCl中-1价,氧元素由-2价升高为O2中0价,转移电子数为12;
(3)反应中Fe元素化合价由+2价升高到+3价,Cl元素化合价由0价降低到-1价;
(4)反应中N元素的化合价由-3升高为0,Cl元素的化合价0降低为-1价,氨气作还原剂,氯气作氧化剂,氯化铵为还原产物,被氧化的氨气:参加反应的氨气之比为1:4.
解答 解:(1)反应中H2S中S氧化化合价升高,由-2价升高到0价,SO2中S元素化合价降低,由+4价降低到0价,氧化还原反应反应中得失电子数目相等,表现为化合价升降的总数相等,为 ,故答案为:
,故答案为: ;
;
(2)应中Cl元素化合价由+5价降低为KCl中-1价,氧元素由-2价升高为O2中0价,转移电子数为12,用单线桥表示电子转移的情况为: ,氧化产物和还原产物的物质的量之比为3:2,
,氧化产物和还原产物的物质的量之比为3:2,
故答案为: ;3:2;
;3:2;
(3)反应中Fe元素化合价由+2价升高到+3价,Cl元素化合价由0价降低到-1价,用单线桥表示电子转移的情况为: ,
,
故答案为: ;
;
(4)反应中N元素的化合价由-3升高为0,Cl元素的化合价0降低为-1价,2molNH3作还原剂转移电子为6mol,则反应电子转移的方向和数目为 ,被氧化的氨气:参加反应的氨气之比为1:4.故答案为:
,被氧化的氨气:参加反应的氨气之比为1:4.故答案为: ;1:4.
;1:4.
点评 本题考查较为综合,全面考查氧化还原反应知识,注意把握元素化合价的变化,明确电子转移的数目和方向,根据化合价的升降总数计算电子转移的数目,题目难度中等.

练习册系列答案
相关题目
4.碱式碳酸铜和氯气都是用途广泛的化工原料.
(1)工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H+、Cl-)制备碱式碳酸铜,其制备过程如下:

已知:Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
①氯酸钠的作用是将Fe2+氧化成Fe3+并最终除去;
②反应A后调节溶液的pH范围应为3.2-4.2.
③第一次过滤得到的产品洗涤时,如何判断已经洗净?取最后一次洗涤液,加入硝酸银、稀硝酸,无沉淀生成则表明已洗涤干净.
④造成蓝绿色产品中混有CuO杂质的原因是反应B的温度过高.
(2)已知在某温度下Fe(OH)3的容度积常数Ksp=[Fe(OH)3]=1.0×10-38,已知在该温度下溶液中Fe3+离子浓度小于1×10-5mol/L时,该离子已沉淀完全.则该沉淀完全所需要的pH为3.3.
(1)工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H+、Cl-)制备碱式碳酸铜,其制备过程如下:

已知:Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 4.2 | 5.8 | 1.2 |
| 完全沉淀pH | 6.7 | 8.3 | 3.2 |
②反应A后调节溶液的pH范围应为3.2-4.2.
③第一次过滤得到的产品洗涤时,如何判断已经洗净?取最后一次洗涤液,加入硝酸银、稀硝酸,无沉淀生成则表明已洗涤干净.
④造成蓝绿色产品中混有CuO杂质的原因是反应B的温度过高.
(2)已知在某温度下Fe(OH)3的容度积常数Ksp=[Fe(OH)3]=1.0×10-38,已知在该温度下溶液中Fe3+离子浓度小于1×10-5mol/L时,该离子已沉淀完全.则该沉淀完全所需要的pH为3.3.
5.25℃时,将pH=2和pH=5的硫酸溶液等体积混合后,溶液的pH为( )
| A. | 2.3 | B. | 4.7 | ||
| C. | 3.5 | D. | 以上答案都不正确 |
2.学生常用的涂改液中含有许多挥发性的有害物质,二氯甲烷(CH2Cl2)是其中的一种.下面有关二氯甲烷的几种说法:
①它是由碳、氢、氯三种元素组成的化合物;
②它是由氯气和甲烷组成的混合物;
③它的分子中碳、氢、氯的原子个数比为1:2:2;
④它是由多种原子构成的混合物.这些说法中正确的是( )
①它是由碳、氢、氯三种元素组成的化合物;
②它是由氯气和甲烷组成的混合物;
③它的分子中碳、氢、氯的原子个数比为1:2:2;
④它是由多种原子构成的混合物.这些说法中正确的是( )
| A. | ①③ | B. | ②④ | C. | ②③④ | D. | ①③④ |
9.下列物质中能导电,且为电解质的是( )
| A. | 酒精 | B. | K2SO4晶体 | C. | 熔融NaCl | D. | Cu |
6.欲除去CO2中的少量SO2,可选用( )
| A. | 饱和Na2CO3溶液 | B. | 饱和NaHCO3溶液 | C. | NaOH | D. | Ca(OH)2 |
 ,反应中NaH作为还原剂.
,反应中NaH作为还原剂. .
.
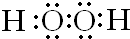 ,C元素在周期表中的位置是第二周期、第ⅦA族.
,C元素在周期表中的位置是第二周期、第ⅦA族.