题目内容
已知NaHSO4在水中的电离方程式为NaHSO4=Na++H++SO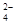 。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,不正确的是( )
。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,不正确的是( )
A.该温度高于25 ℃
B.由水电离出来的H+的浓度是1.0×10-10 mol·L-1
C.NaHSO4晶体的加入抑制了水的电离
D.该温度下加入等体积pH为12的NaOH溶液可使该溶液恰好呈中性
【答案】
D
【解析】
试题分析:pH=6的蒸馏水,说明蒸馏水中氢离子的浓度是1.0×10-6mol·L-1,所以水的离子积常数是1.0×10-12,这说明水的电离是被促进的,因此温度高于25℃,A正确;B中溶液中氢离子浓度是0.01mol/L,则溶液中OH-的浓度就是1.0×10-10 mol·L-1,则由水电离出来的H+的浓度是1.0×10-10 mol·L-1,B正确;硫酸氢钠能电离出氢离子,抑制水的电离,C正确;D中氢氧化钠的浓度是1mol/L,所以反应后氢氧化钠是过量的,溶液显碱性,D不正确,答案选D。
考点:考查外界条件对水的电离平衡的影响、离子浓度计算以及溶液酸碱性的判断
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,贴近高考,有利于考查学生的逻辑推理能力和灵活应变能力。该题的关键是明确该温度下水的离子积常数的变化,然后再结合题意灵活分析即可得出正确的结论。

练习册系列答案
相关题目
已知NaHSO4 在水中的电离方程式为:NaHSO4=Na++H++SO42-,某温度下,向pH=6的纯水中加入NaHSO4 晶体,保持温度不变,测得溶液的pH为2.下列对该溶液的叙述中,不正确的是( )
| A、该温度高于25℃ | B、由水电离出来的H+ 的浓度是1.0×10-10mol?L-1 | C、该温度下加入等体积pH=12 的NaOH 溶液可使该溶液恰好呈中性 | D、NaHSO4晶体的加入抑制了水的电离 |