��Ŀ����
6��X��Y��Z��W�����ֽ������ʣ���X����Z����������Һ�У�X�ı�����Z������X��Y��ϡ�������ԭ���ʱ��X�缫�����������ɣ�Z��W�����Ӻ����ϡ�����У�������Z����W��X��Y��Z���ֽ����Ļ��˳��Ϊ��������| A�� | Y��X��Z��W | B�� | W��X��Z��Y | C�� | X��Y��Z��W | D�� | Y��Z��X��W |
���� �ڽ����Ļ��˳���������ǰ��Ľ����ܰ�������Ľ�����������Һ���û�������
�����ֽ�����ϡ������ɵ�ԭ����У��ϻ��õĽ������������ϲ����õĽ�����������������ʧ���ӷ���������Ӧ�������������ӵõ��ӷ�����ԭ��Ӧ�������������ӴӸ����ص��������������ݴ˷������
��� �⣺��X����Z����������Һ�У�X�ı�����Z��������֪��������˳��ΪX��Z��
X��Y��ϡ�������ԭ���ʱ��X�缫�����������ɣ�˵��XΪ��������������˳��ΪY��X��
Z��W�����Ӻ����ϡ�����У�������Z����W��˵��ZΪ��������������˳��ΪZ��W��
�����ֽ����Ļ��˳����Y��X��Z��W��
��ѡA��
���� �����Խ������˳����ж�Ϊ���忼����ԭ��صĹ���ԭ�������ݽ����Ļ����ԡ��缫��Ӧ���͡��缫��Ӧ�����֪ʶ��������ɣ���Ŀ�ѶȲ���

��ϰ��ϵ�д�
�����Ŀ
16�����й�ϵ�ı����У���ȷ���ǣ�������
| A�� | �ֱ�CuSO4��Na2CO3��KNO3��Ca��HCO3��2��FeCl3�ı�����Һ���ȡ�������Ũ������ȴ�����ܵõ���ԭ���������ͬ�ľ�����CuSO4��KNO3 | |
| B�� | �к�pH���������ͬ������ʹ��ᣬ����NaOH�����ʵ���֮��Ϊ1��1 | |
| C�� | pH=3�������pH=3��FeCl3��Һ�У�ˮ�����c��H+������� | |
| D�� | 0.1 mol/L NaHCO3��Һ�У�c��Na+����c��HCO3-����c��CO32-����c��H2CO3�� |
17�����з�Ӧ���ڷ��ȷ�Ӧ���ǣ�������
| A�� | C��ˮ�����ڸ����·�Ӧ��ȡˮú�� | |
| B�� | CO2��C�ڸ����½��з�Ӧ | |
| C�� | ���ȷֽ�̼��� | |
| D�� | ����ˮ�ķ�Ӧ |
14������Ԫ�ص�ԭ�Ӱ뾶���μ�С���ǣ�������
| A�� | Na��Mg��Al | B�� | N��P��As | C�� | P��Si��Al | D�� | C��Si��P |
11���������ʼ��ת�����ܾ���һ�����Ϸ�Ӧֱ��ת�����ǣ�������
| A�� | SiO2��H2SiO3 | B�� | Na2O2��Na2CO3 | C�� | Cu��Cu2��OH��2CO3 | D�� | AlCl3��Al��OH��3 |
18�����Ĵ��������ǹ�ҵ��������ȡ�������Ҫ;��������Ϊ���е�һ����Ҫ��Ӧ��
4H3��g��+5O2��g��?4NO��g��+6H2O��g��
���������£���Ӧ���������ǣ�������
4H3��g��+5O2��g��?4NO��g��+6H2O��g��
���������£���Ӧ���������ǣ�������
| ѡ�� | �¶� | ���� | NH3��g��Ũ�� |
| A | 500�� | ����Ͻ��� | 2mol/L |
| B | 500�� | �� | 1mol/L |
| C | 800�� | ����Ͻ��� | 2mol/L |
| D | 800�� | ����Ͻ��� | 1mol/L |
| A�� | A | B�� | B | C�� | C | D�� | D |
10�����жԳ��л�ѧ֪ʶ���ܽᣬ������ǣ�������
| A�� | ��ѧ������Ӧ���Ͱ������Ϸ�Ӧ���ֽⷴӦ���û���Ӧ���ֽⷴӦ���� | |
| B�� | �������Ӫ�����ǵ����ʡ����ࡢ��֬��ά���ء����κ�ˮ | |
| C�� | ��ͬ��Ԫ����ɵ�����һ���Ǵ����� | |
| D�� | ��������ʱ����ʪë����ס�ڱǣ�������������ֳ� |
11������H2S��NH3��CH4�������壬���Ƿֱ�����ͬ��Ŀ����ԭ�ӣ���������������ʵ���֮��Ϊ��������
| A�� | 1��1��1 | B�� | 2��3��4 | C�� | 6��4��3 | D�� | 6��3��4 |
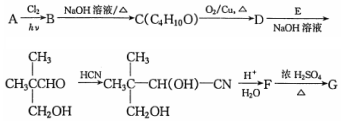
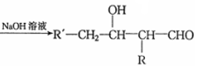
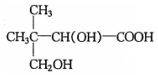 $��_{��}^{Ũ����}$
$��_{��}^{Ũ����}$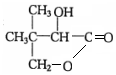 +H2O��F�ܷ������۷�Ӧ�����������ڵ����������ĸ�̼Ը�ӵĸ߷��ӻ�����Ľṹ��ʽΪ
+H2O��F�ܷ������۷�Ӧ�����������ڵ����������ĸ�̼Ը�ӵĸ߷��ӻ�����Ľṹ��ʽΪ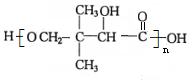 ��
��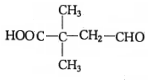 ��
��