题目内容
在一恒温恒容的密闭容器中,发生如下反应:2A(g)+B(g) nC(g)若Ⅰ在容器中充入2molA和1molB作为起始物质,达平衡后C的体积分数为X%.
nC(g)若Ⅰ在容器中充入2molA和1molB作为起始物质,达平衡后C的体积分数为X%.
Ⅱ.若在Ⅰ达到平衡后,再向容器中充入2molA和1molB,平衡向移动,达到新平衡后C的体积分数为Y%.则:
(1)当n>3时,X%________y%.(比较大小)
(2)当n=3时,X%________y%.
(3)当n<3时,X%________y%.
答案:略
解析:
解析:
|
比较两个化学平衡可知:Ⅱ分两次共加入 4molA和2molB,即起始浓度Ⅱ恰好为Ⅰ的两倍,根据勒夏特列原理,增大反应物浓度,平衡向正反应方向移动,则达新平衡后C物质的量增大,但混合气体总物质的量也增大,因而达新平衡后C的体积分数如何改变难以确定.平衡Ⅱ A、B起始浓度均为平衡Ⅰ的2倍;若仍以Ⅰ中2molA和1molB作为起始物质,只需将容器体积压缩至原来的一半,A、B浓度同样增大到原来的两倍,从而将浓度的变化转换为压强的变化,根据勒夏特列原理:(1)当n>3时,增大压强,平衡向逆反应方向移动,则X%>y%; (2)当n=3时,增大压强,平衡不移动,则X%=y%; (3)当n<3时,增大压强,平衡向正反应方向移动,则X%<y%. |

练习册系列答案
 名题金卷系列答案
名题金卷系列答案
相关题目
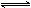 nC(g)若Ⅰ在容器中充入2molA和1molB作为起始物质,达平衡后C的体积分数为X%.
nC(g)若Ⅰ在容器中充入2molA和1molB作为起始物质,达平衡后C的体积分数为X%.
 2SO3(g)△H=-196.6kJ?mol-1,在一恒温恒容容器中投入一定量的SO2和O2,经过一段时间一定能证明该反应已达平衡状态的是______.
2SO3(g)△H=-196.6kJ?mol-1,在一恒温恒容容器中投入一定量的SO2和O2,经过一段时间一定能证明该反应已达平衡状态的是______.


 2SO3(g)△H=-196.6kJ?mol-1,在一恒温恒容容器中投入一定量的SO2和O2,经过一段时间一定能证明该反应已达平衡状态的是______.
2SO3(g)△H=-196.6kJ?mol-1,在一恒温恒容容器中投入一定量的SO2和O2,经过一段时间一定能证明该反应已达平衡状态的是______.