题目内容
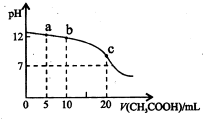
右图是用0.1mol?L-1 CH3COOH溶液滴定20mL 0.1mol?L-1NaOH溶液的滴定曲线.该溶液中有关粒子浓度的关系式不正确的是( )
A.当pH=7时:c(Na+)=c(CH3COO-)>c(OH-)=c(H+)
B.在a点时:c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
C.在b点时:c(OH-)=c(H-)+c(CH3COO-)+2c(CH3COOH)
D.在c点时:c(Na+)+c(H+)+c(CH3COOH)-c(OH-)=0.05mol?L-1
【答案】分析:A、PH=7时,c(OH-)=c(H+),根据溶液电中性可判断c(Na+)=c(CH3COO-);
B、在a点时,NaOH过量c(Na+)>c(CH3COO一);
C、在b点时,根据溶液电中性和加入醋酸的物质的量以及NaOH的物质的量进行分析;
D、在c点时,根据加入醋酸的物质的量以及溶液电中性进行分析.
解答:解:A、PH=7时,c(OH-)=c(H+),根据溶液电中性可判断c(Na+)=c(CH3COO-),此时溶液中c(Na+)稍小于0.05mol/L,而c(OH-)=1×10-7mol/L,则c(Na+)>c(OH-),所以有
c(Na+)=c(CH3COO-)>c(OH-)=c(H+),故A正确;
B、在a点时,加入醋酸为5ml,NaOH过量c(Na+)>c(CH3COO-),故B错误;
C、在b点时,加入醋酸为10ml,溶液中c(CH3COO-)+c(CH3COOH)=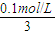 ,c(Na+)=
,c(Na+)=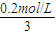 ,即c(Na+)=2c(CH3COO-)+2c(CH3COOH),溶液中存在c(Na+)+c(H+)=c(OH-)+c(CH3COO-),则有2c(CH3COO-)+2c(CH3COOH)+c(H+)=c(OH-)+c(CH3COO-),即c(OH-)=c(H-)+c(CH3COO-)+2c(CH3COOH),故C正确;
,即c(Na+)=2c(CH3COO-)+2c(CH3COOH),溶液中存在c(Na+)+c(H+)=c(OH-)+c(CH3COO-),则有2c(CH3COO-)+2c(CH3COOH)+c(H+)=c(OH-)+c(CH3COO-),即c(OH-)=c(H-)+c(CH3COO-)+2c(CH3COOH),故C正确;
D、在c点时,加入醋酸为20ml,两种溶液等体积混合,溶液中c(CH3COO-)+c(CH3COOH)=0.05mol?L-1,c(Na+)=0.05mol?L-1,
则有c(CH3COO-)=0.05mol?L-1-c(CH3COOH),溶液中存在c(Na+)+c(H+)=c(OH-)+c(CH3COO-),则有c(Na+)+c(H+)=c(OH-)+0.05mol?L-1-c(CH3COOH),所以有c(Na+)+c(H+)+c(CH3COOH)-c(OH-)=0.05mol?L-1,故D正确.
故选B.
点评:本题考查溶液中离子浓度大小比较,做题时注意分析图象判断溶液反应的程度,注意溶液电中性的巧妙利用,题目难度中等.
B、在a点时,NaOH过量c(Na+)>c(CH3COO一);
C、在b点时,根据溶液电中性和加入醋酸的物质的量以及NaOH的物质的量进行分析;
D、在c点时,根据加入醋酸的物质的量以及溶液电中性进行分析.
解答:解:A、PH=7时,c(OH-)=c(H+),根据溶液电中性可判断c(Na+)=c(CH3COO-),此时溶液中c(Na+)稍小于0.05mol/L,而c(OH-)=1×10-7mol/L,则c(Na+)>c(OH-),所以有
c(Na+)=c(CH3COO-)>c(OH-)=c(H+),故A正确;
B、在a点时,加入醋酸为5ml,NaOH过量c(Na+)>c(CH3COO-),故B错误;
C、在b点时,加入醋酸为10ml,溶液中c(CH3COO-)+c(CH3COOH)=
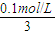 ,c(Na+)=
,c(Na+)=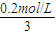 ,即c(Na+)=2c(CH3COO-)+2c(CH3COOH),溶液中存在c(Na+)+c(H+)=c(OH-)+c(CH3COO-),则有2c(CH3COO-)+2c(CH3COOH)+c(H+)=c(OH-)+c(CH3COO-),即c(OH-)=c(H-)+c(CH3COO-)+2c(CH3COOH),故C正确;
,即c(Na+)=2c(CH3COO-)+2c(CH3COOH),溶液中存在c(Na+)+c(H+)=c(OH-)+c(CH3COO-),则有2c(CH3COO-)+2c(CH3COOH)+c(H+)=c(OH-)+c(CH3COO-),即c(OH-)=c(H-)+c(CH3COO-)+2c(CH3COOH),故C正确;D、在c点时,加入醋酸为20ml,两种溶液等体积混合,溶液中c(CH3COO-)+c(CH3COOH)=0.05mol?L-1,c(Na+)=0.05mol?L-1,
则有c(CH3COO-)=0.05mol?L-1-c(CH3COOH),溶液中存在c(Na+)+c(H+)=c(OH-)+c(CH3COO-),则有c(Na+)+c(H+)=c(OH-)+0.05mol?L-1-c(CH3COOH),所以有c(Na+)+c(H+)+c(CH3COOH)-c(OH-)=0.05mol?L-1,故D正确.
故选B.
点评:本题考查溶液中离子浓度大小比较,做题时注意分析图象判断溶液反应的程度,注意溶液电中性的巧妙利用,题目难度中等.

练习册系列答案
相关题目
 右图是用0.1mol?L-1 CH3COOH溶液滴定20mL 0.1mol?L-1NaOH溶液的滴定曲线.该溶液中有关粒子浓度的关系式不正确的是( )
右图是用0.1mol?L-1 CH3COOH溶液滴定20mL 0.1mol?L-1NaOH溶液的滴定曲线.该溶液中有关粒子浓度的关系式不正确的是( ) CH3OH(g)△H1=-116kJ?molˉ1
CH3OH(g)△H1=-116kJ?molˉ1
 化的曲线图,请指明图中的压强P1=
化的曲线图,请指明图中的压强P1= CO(g)+2H2(g)反应的平衡常数为
CO(g)+2H2(g)反应的平衡常数为