题目内容
(共16分) 硫化钠是用于皮革鞣制的重要化学试剂,可用无水芒硝(Na2SO4)与炭粉在高温下反应而制得,反应式如下:
① Na2SO4 4C
4C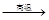 Na2S
Na2S 4CO↑
4CO↑
② Na2SO4 4CO
4CO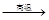 Na2S
Na2S 4CO2
4CO2
(1)、现要制取Na2S 7.80 g,若生产过程中无水芒硝(Na2SO4)的利用率为90%,则理论上需要无水芒硝(Na2SO4) g(精确到0.01);
(2)、若在反应中生成的Na2S物质的量为1 mol,则消耗的碳单质的物质的量n的范围是
<n< ;
(3)、若在上述反应中消耗的碳单质为1 mol,生成Na2S的物质的量为 y mol,生成的CO和CO2的物质的量之比为x,则y与x的关系式为y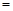 ;
;
(4)、Na2S放置在空气中,会缓慢氧化成Na2SO3及Na2SO4,现称取已经部分氧化的硫化钠样品39.20 g溶于水中,加入足量硫酸,充分反应后,过滤得沉淀9.6 g,放出H2S气体1.12 L(标准状况)。请计算:39.20 g样品中各成分的物质的量分别为 。
(请写出计算过程)
(1).15.78 (2分) (2).2 mol ~ 4 mol。(4分) (3).y =(x+2)/4(1+x) (4分) (4).n(Na2S)="0.25" mol n(Na2SO3)="0.10" mol n(Na2SO4)="0.05" mol
解析

(每空2分,共16分)下表是元素周期表的一部分,请回答有关问题:
|
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | ||||||
| 2 |
|
|
| ① | ② |
| ③ |
| ||||||
| 3 |
| ④ | ⑤ |
|
| ⑥ | ⑦ | ⑧ | ||||||
| 4 | ⑨ |
|
|
|
|
| ⑩ |
|
(1)表中化学性质最不活泼的元素,其原子结构示意图为 。
(2)表中能形成两性氢氧化物的元素是 (用元素符号表示),写出该元素的单质与⑨最高价氧化物的水化物反应的化学方程式 。![]()
(3)④元素与⑦元素形成化合物的电子式 。
(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是 (填化学式)。
(5)③元素与⑩元素两者核电荷数之差是 。
(6)在⑦与⑩的单质中,化学性质较活泼的物质名称是 ,可用什么化学反应说明该事实(写出反应的化学方程式): 。
(每空2分,共16分)下表是元素周期表的一部分,请回答有关问题:
|
|
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
||||||
|
2 |
|
|
|
① |
② |
|
③ |
|
||||||
|
3 |
|
④ |
⑤ |
|
|
⑥ |
⑦ |
⑧ |
||||||
|
4 |
⑨ |
|
|
|
|
|
⑩ |
|
(1)表中化学性质最不活泼的元素,其原子结构示意图为 。
(2)表中能形成两性氢氧化物的元素是 (用元素符号表示),写出该元素的单质与⑨最高价氧化物的水化物反应的化学方程式 。
(3)④元素与⑦元素形成化合物的电子式 。
(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是 (填化学式)。
(5)③元素与⑩元素两者核电荷数之差是 。
(6)在⑦与⑩的单质中,化学性质较活泼的物质名称是 ,可用什么化学反应说明该事实(写出反应的化学方程式): 。
 CH3CH2CH2CHO
CH3CH2CH2CHO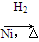 CH3CH2CH2CH2OH:
CH3CH2CH2CH2OH: CO↑+H2O,并设计出原料气的制备装置(如图)。
CO↑+H2O,并设计出原料气的制备装置(如图)。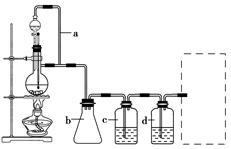
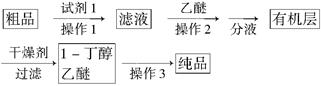
 4C
4C Na2S
Na2S ;
; 