题目内容
下列溶液经反应后,溶液内含有0.50mol NaHCO3和0.50mol Na2CO3的是( )
| A、0.50L 1.00 mol?L-1 NaHCO3加0.50L 0.50 mol?L-1 NaOH | B、0.50L 0.75 mol?L-1 Na2CO3加0.50L 0.50 mol?L-1 HCl | C、0.50L 1.00 mol?L-1 NaHCO3 加0.50L 0.25 mol?L-1 NaOH | D、1.00L 1.00 mol?L-1 Na2CO3 加1.00L 0.50 mol?L-1 HCl |
分析:根据方程式:NaHCO3+NaOH═Na2CO3+H2O,Na2CO3+HCl═NaHCO3+NaCl,结合题目中的物质的量计算.
解答:解:A、0.50L 1.00 mol?L-1NaHCO3中n(NaHCO3)=0.50mol,加入0.50L 0.50 mol?L-1NaOH,发生NaHCO3+NaOH═Na2CO3+H2O,则生成n(Na2CO3)=0.25mol,不符合题意,故A不选;
B、0.50L 0.75 mol?L-1 Na2CO3中n(Na2CO3)=0.375mol,加0.50L 0.50 mol?L-1 HCl,发生Na2CO3+HCl═NaHCO3+NaCl,则生成n(NaHCO3)=0.25mol,不符合题意,故B不选;
C、0.50L 1.00 mol?L-1 NaHCO3 中n(NaHCO3)=0.5mol,加0.50L 0.25 mol?L-1 NaOH,发生NaHCO3+NaOH═Na2CO3+H2O,则生成n(Na2CO3)=0.125mol,不符合题意,故C不选;
D、1.00L 1.00 mol?L-1 Na2CO3 n(Na2CO3)=1.00mol,加1.00L 0.50 mol?L-1 HCl,发生Na2CO3+HCl═=NaHCO3+NaCl,则n(HCl)=0.50mol,所以生成n(NaHCO3)=0.50mol,剩余的n(Na2CO3)=0.50mol,故符合题意,故D选;
故选:D.
B、0.50L 0.75 mol?L-1 Na2CO3中n(Na2CO3)=0.375mol,加0.50L 0.50 mol?L-1 HCl,发生Na2CO3+HCl═NaHCO3+NaCl,则生成n(NaHCO3)=0.25mol,不符合题意,故B不选;
C、0.50L 1.00 mol?L-1 NaHCO3 中n(NaHCO3)=0.5mol,加0.50L 0.25 mol?L-1 NaOH,发生NaHCO3+NaOH═Na2CO3+H2O,则生成n(Na2CO3)=0.125mol,不符合题意,故C不选;
D、1.00L 1.00 mol?L-1 Na2CO3 n(Na2CO3)=1.00mol,加1.00L 0.50 mol?L-1 HCl,发生Na2CO3+HCl═=NaHCO3+NaCl,则n(HCl)=0.50mol,所以生成n(NaHCO3)=0.50mol,剩余的n(Na2CO3)=0.50mol,故符合题意,故D选;
故选:D.
点评:本题考查了碳酸钠与碳酸氢钠的转化,以及有关物质的量的计算,题目比较简单.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 溴苯是一种化工原料,实验室合成溴苯的装置示意图如图及有关数据如下:按下列合成步骤回答问题:
溴苯是一种化工原料,实验室合成溴苯的装置示意图如图及有关数据如下:按下列合成步骤回答问题: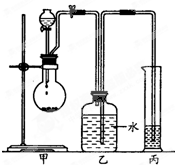 某化学小组探究液体有机物样品A(C3H8O2)的结构,进行如下实验.
某化学小组探究液体有机物样品A(C3H8O2)的结构,进行如下实验.