��Ŀ����
����Ȼ��Ϊԭ�Ϻϳ����ص������е���Ҫ��Ӧ֮һΪCH4(g)+H2O(g)![]() CO(g)+3H2(g)����H��0
CO(g)+3H2(g)����H��0
�������ĿҪ��ش��������⡣
(1)��һ�������£���0.05molCH4��0.10molH2O�������ݻ�
(2)�������������������½����¶ȣ����淴Ӧ����__________(�������С�����䡱����ͬ)���������������������¼�ѹ��������Ӧ����____________________��
(3)��һ�������£����÷�Ӧ���ڻ�ѧƽ��״̬ʱ�����в�����ʹ��ѧƽ��������Ӧ�����ƶ�����__________(�����)��
A.�����¶� B.�����¶� C.����ѹǿ D.��Сѹǿ E.������� F.�Ƴ�ˮ����
(4)��һ���¶��£���1.0 mol CH4��2.0molH2O(g)ͨ��ijһ��ѹ�����У��ﵽ��ѧƽ��ʱ���������4.0mol����CH4��ת����Ϊ___________���������������䣬��ʼʱ����amol CH4��bmol H2O(g)��cmolCO��dmolH2���ﵽƽ��ʱ��������������������ƽ����ȫ��ȣ���a��b��c����Ĺ�ϵΪ___________(����ĸ��ʾ)��
(1)![]() =7.5��10-4mol��(L��s)-1��
=7.5��10-4mol��(L��s)-1��![]() ��10-3mol��(L��s)-1��0.00075mol��(L��s)-1(ע����д��λ����)
��10-3mol��(L��s)-1��0.00075mol��(L��s)-1(ע����д��λ����)
(2)��С ����
(3)A��D
(4)50��
�����������⿼���˻�ѧ��Ӧ����v�ļ��㣬Ӱ��v�����ؼ���ѧƽ�����أ���Чƽ�⡣v(H2)=3v(CO)=![]() ��3=7.5��10-4mol��(L��s)-1��
��3=7.5��10-4mol��(L��s)-1��
��Ϊ�¶Ⱥ�ѹǿ��v����v����Ӱ����ͬʱ�����С����˶Դ˷�Ӧ���£�v����С����ѹv���������ڦ�H��0��������Ϊ���ȷ�Ӧ����Ӧ�����廯ѧ������С�������ﻯѧ��������������Ϊ�������ķ�Ӧ������A��D���ϡ���CH4��ת���ʣ�Ҫ��CH4��Ӧ�����ʵ�������CH4��Ӧ�����ʵ���Ϊx��
CH4 + H2O ![]() CO+3H2
CO+3H2
��ʼ��1.0mol 2.0mol 0 0
ƽ�⣺(1.0mol-x) (2.0-x) x 3x
��x=0.5mol
ת����Ϊ![]() ��100��=50����
��100��=50����
���ݵ�Чƽ��

����[CO(NH2)2]��һ�ַdz���Ҫ�ĸߵ�����,����Ȼ������H2S)Ϊԭ�� �ϳ����ص���Ҫ��������ͼ��ʾ��ͼ��ijЩת������δ�г�����

��ش��������⣺
��1����Ӧ�ٵ����ӷ���ʽ��______________
��2����Ȼ������������Fe2S3��H2O��02��Ӧ�Ļ�ѧ����ʽ��_______��
��3����Ӧ���Ƿ��ȷ�Ӧ���¶����ߣ��÷�Ӧ��ƽ�ⳣ��_______ (�� ����������С�� ���䡱)��H2NCOONH4 (��������泥��Ǻϳ����ص��м��壬����̼ԭ�ӵ��ӻ����������_______�ӻ���
��4����������������������ɫ��ѧ���գ������� 120t������������Ҫ CH4___m3 (��״������
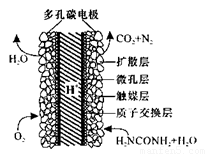
��5����ѧ�������о����ض���ȼ�ϵ�أ���ҺҲ�ܷ��磡�����ֵ��ֱ��ȥ�����з�ˮ�е����أ����ܲ���������ˮ���ܷ��硣����ȼ�ϵ�ؽṹ��ͼ��ʾ������ʱ�����ĵ缫��ӦʽΪ__________