题目内容
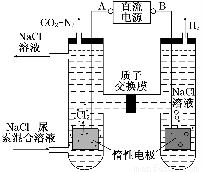
尿素[CO(NH2)2]是一种非常重要的高氮化肥,以天然气(含H2S)为原料 合成尿素的主要步骤如下图所示(图中某些转化步骤未列出)。

请回答下列问题:
(1)反应①的离子方程式是______________
(2)天然气脱硫后产生的Fe2S3和H2O与02反应的化学方程式是_______。
(3)反应②是放热反应,温度升高,该反应的平衡常数_______ (填 “增大”、“减小” 或“不变”)。H2NCOONH4 (氨基甲酸铵)是合成尿素的中间体,其中碳原子的杂化轨道类型是_______杂化。
(4)如果整个生产过程釆用绿色化学工艺,则生产 120t尿素理论上需要 CH4___m3 (标准状况)。
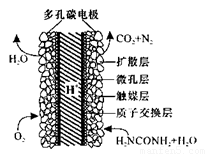
(5)化学家正在研究尿素动力燃料电池,尿液也能发电!用这种电池直接去除城市废水中的尿素,既能产生净化的水又能发电。尿素燃料电池结构如图所示,工作时负极的电极反应式为__________
(14分)
(1)CO32-+CO2+H2O=2HCO3-(2分)
(2)2Fe2S3+6H2O+3O2=4Fe(OH)3+6S(2分)
(3)减小(2分) sp2(2分) (4)4.48×104(3分)
(5)CO(NH2)2+H2O-6e-= N2↑+CO2↑+6H+(3分)
【解析】
试题分析:(1)反应①发生二氧化碳与碳酸钾溶液反应生成碳酸氢钾,其离子反应为CO32-+CO2+H2O═2HCO3-;(2)Fe2S3和H2O与02反应生成氢氧化铁和S,该反应为2Fe2S3+6H2O+3O2═4Fe(OH)3+6S;(3)反应②为合成氨的反应,放热反应,温度升高,平衡逆向移动,则平衡常数K减小;H2NCOONH4中的C原子上没有孤对电子,成键数为3,C原子采取sp2杂化;(4)由C原子守恒可知,CH4~CO2~CO(NH2)2,则生产120t尿素理论上需要CH4为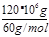 ×22.4L/mol×10-3m3=4.48×104m3;(5)尿素燃料电池中尿素再负极上失去电子生成氮气、二氧化碳,负极反应为CO(NH2)2+H2O-6e-═N2↑+CO2↑+6H+;
×22.4L/mol×10-3m3=4.48×104m3;(5)尿素燃料电池中尿素再负极上失去电子生成氮气、二氧化碳,负极反应为CO(NH2)2+H2O-6e-═N2↑+CO2↑+6H+;
考点:本题以尿素的合成为信息考查化学用语及化学平衡、电化学等知识,综合性较强,题目难度中等,第(5)问为学生解答的难点和易错点。

下列说法错误的是
| A.清晨茂密树林中缕缕阳光穿过枝叶铺洒在地面形成的美丽景色与胶体的性质有关 |
| B.元素周期律是元素原子核外电子排布随着元素核电荷数的递增发生周期性变化的必然结果 |
| C.尿素[CO(NH2)2]的合成突破了无机物和有机物的界限,人们用含碳无机物为原料合成了大量的有机物,创造了一个新的“自然界” |
| D.Na2CO3俗名小苏打,是焙制糕点所用发酵粉的主要成分之一 |
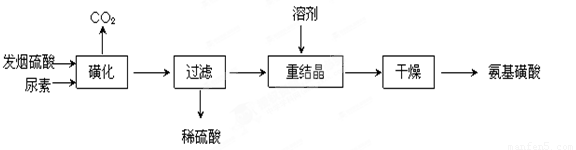
 H2NCONHSO3H(s)
△H<0
H2NCONHSO3H(s)
△H<0