题目内容
15.3.01×1023个CO2在标准状况下的体积为11.2L,质量是22g.分析 根据n=$\frac{N}{{N}_{A}}$计算3.01×1023个CO2的物质的量,根据V=nVm计算CO2的体积,根据m=nM计算CO2的质量.
解答 解:3.01×1023个CO2的物质的量为:$\frac{3.01×1{0}^{23}}{6.02×1{0}^{23}mo{l}^{-1}}$=0.5mol,
0.5molCO2的体积为:0.5mol×22.4L/mol=11.2L,
0.5molCO2的质量为:0.5mol×44g/mol=22g,
故答案为:11.2L; 22g.
点评 本题考查常用化学计量的有关计算,比较基础,注意公式的理解与灵活运用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.某溶液经分析,其中只含Na+、K+、Mg2+、Cl-、SO42-,已知其中Na+、K+、Mg2+、Cl-的浓度均为0.1mol•L-1,则SO42- 的物质的量浓度为( )
| A. | 0.1 mol•L-1 | B. | 0.15 mol•L-1 | C. | 0.2 mol•L-1 | D. | 0.3 mol•L-1 |
3.下列各组性质的比较中,不正确的是( )
| A. | 碱性:NaOH>Mg(OH)2 | B. | 热稳定性:HCl>HBr | ||
| C. | 失电子能力:K>Na | D. | 原子半径:CI>S |
20.以NA表示阿伏伽德罗常数,下列说法中正确的是( )
| A. | 58.5 g氯化钠固体中含有NA个氯化钠分子 | |
| B. | 1mol Fe参与反应失去电子数目一定为2NA | |
| C. | 金属钠和氧气反应制取过氧化钠,每生成1mol过氧化钠,转移电子数为4NA | |
| D. | 常温下,46 g NO2和N2O4的混合物中含有的氮原子数为NA |
5.关于实验事故或药品的处理方法中,正确的是( )
| A. | 少量浓硫酸沾在皮肤上,立即用大量氢氧化钠溶液冲洗 | |
| B. | 大量氯气(溶于水显酸性)泄漏时,用肥皂水浸湿毛巾捂住嘴和鼻,并迅速离开现场 | |
| C. | 不慎洒出的酒精在桌上着火时,应立即用大量水扑灭 | |
| D. | 实验室发生火灾时,应立即打开门窗呼救 |
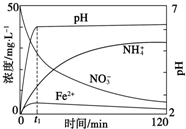 工、农业废水及生活污水中浓度较高的NO${\;}_{3}^{-}$会造成氮污染,工业上处理水体中NO${\;}_{3}^{-}$的一种方法是单质铁化学还原法.某化学小组用废铁屑和硝酸盐溶液模拟此过程,实验如下.
工、农业废水及生活污水中浓度较高的NO${\;}_{3}^{-}$会造成氮污染,工业上处理水体中NO${\;}_{3}^{-}$的一种方法是单质铁化学还原法.某化学小组用废铁屑和硝酸盐溶液模拟此过程,实验如下.