题目内容
相关数据如下表

- A.△H =+102kJ/mol
- B.△H =-102kJ/mol
- C.△H =+267kJ/mol
- D.△H =-267kJ/mol
B
反应热是断键吸收的能量和形成化学键所放出的能量的差值,所以该反应的焓变为△H=436 kJ/mol+200 kJ/mol-2×369 kJ/mol=-102 kJ/mol,所以答案是B。
反应热是断键吸收的能量和形成化学键所放出的能量的差值,所以该反应的焓变为△H=436 kJ/mol+200 kJ/mol-2×369 kJ/mol=-102 kJ/mol,所以答案是B。

练习册系列答案
相关题目
已知1g氢气完全燃烧生成液态水时放出热量143kJ,18g水蒸气变成液态水放出44kJ的热量.其它相关数据如下表:
|
已知2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ/mol,蒸发1mol H2O(l)需要吸收的能量为44kJ,其他相关数据如下表:则表中a为( )
| H-H | O═O | H-O | |
| 键能(kJ/mol) | 436.4 | a | 462.8 |
| A、185.2 | B、224.0 |
| C、518.8 | D、494 |
化学平衡状态I、II、Ⅲ的相关数据如下表:
根据以上信息判断,下列结论错误的是( )
| 编号 | 化学方程式 | 平衡常数 | 温度 | |
| 979K | 1173K | |||
| Ⅰ | Fe(s)+CO2?FeO(s)+CO(g) | K1 | 1.47 | 2.15 |
| Ⅱ | CO(g)+H2O(g)?CO2(g)+H2(g) | K2 | 1.62 | b |
| Ⅲ | Fe(s)+H2O(g)? FeO(s)+H2(g) |
K3 | a | 1.68 |
| A、a>b |
| B、增大压强;平衡状态II不移动 |
| C、升高温度平衡状态Ⅲ向正反应方向移动 |
| D、反应Ⅱ,Ⅲ均为放热反应 |
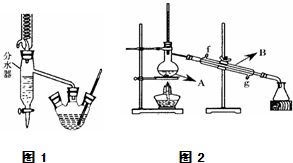 实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表.
实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表.