题目内容
室温下,往0.1mol/L的氨水中滴入酚酞试液时,溶液将呈现粉红色.现采取下列措施,滴有酚酞的氨水溶液颜色不会变浅的是( )
| A、往溶液中滴入稀硫酸 |
| B、往溶液中加入NH4Cl晶体 |
| C、把溶液加热至沸腾 |
| D、往溶液中加入NaOH固体 |
考点:弱电解质在水溶液中的电离平衡,盐类水解的应用
专题:电离平衡与溶液的pH专题
分析:氨水中存在NH3?H2O?NH4++OH-,溶液呈弱碱性,如采取某些措施,滴有酚酞的氨水溶液颜色不会变浅,说明OH-离子浓度不减小,以此解答该题.
解答:
解:A.往溶液中滴入稀硫酸,发生中和反应,OH-离子浓度减小,滴有酚酞的氨水溶液颜色变浅,故A错误;
B.溶液中加入NH4Cl晶体,NH4+浓度增大,抑制NH3?H2O的电离,OH-离子浓度减小,滴有酚酞的氨水溶液颜色变浅,故B错误;
C.把溶液加热至沸腾,氨气挥发,浓度降低,OH-离子浓度减小,滴有酚酞的氨水溶液颜色变浅甚至无色,故C错误;
D.往溶液中加入NaOH固体,OH-离子浓度增大,颜色加深,故D正确.
故选D.
B.溶液中加入NH4Cl晶体,NH4+浓度增大,抑制NH3?H2O的电离,OH-离子浓度减小,滴有酚酞的氨水溶液颜色变浅,故B错误;
C.把溶液加热至沸腾,氨气挥发,浓度降低,OH-离子浓度减小,滴有酚酞的氨水溶液颜色变浅甚至无色,故C错误;
D.往溶液中加入NaOH固体,OH-离子浓度增大,颜色加深,故D正确.
故选D.
点评:本题考查了弱电解质在溶液中的电离,为高考高频考点,侧重于学生的分析能力和基本理论知识的综合理解和运用的考查,题目多角度考查电离平衡,注意把握相关基础知识,难度不大.

练习册系列答案
相关题目
 意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子,N4分子结构与白磷(P4)相同,如图所示,已知断裂1molN-N键吸收167KJ能量,生成1molN≡N放出942KJ能量,根据以上信息和数据判断下列说法正确的是( )
意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子,N4分子结构与白磷(P4)相同,如图所示,已知断裂1molN-N键吸收167KJ能量,生成1molN≡N放出942KJ能量,根据以上信息和数据判断下列说法正确的是( )| A、N4分子是一种新型化合物 |
| B、N4和N2互为同素异形体 |
| C、N4分子的沸点比白磷分子的高 |
| D、1molN4转变为N2将吸收882KJ的能量 |
只用一种试剂就可将甲苯、己烯、四氯化碳、乙醇、KI溶液、H2S水溶液区别开的试剂是( )
| A、KMnO4酸性溶液 |
| B、溴水 |
| C、碘水 |
| D、AgNO3溶液 |
下列有关实验操作或判断正确的是 ( )
| A、用10mL量筒准确量取稀硫酸溶液8.0mL |
| B、用湿润的pH试纸测定氨水的pH |
| C、实验室制备乙烯气体时,将温度计水银球置于混合溶液的液面上方 |
| D、将饱和FeCl3溶液滴入蒸馏水中即得Fe(OH)3胶体 |
| E、圆底烧瓶、锥形瓶、蒸发皿加热时都应垫石棉网. |
常温时,将500mL pH=a的CuSO4和K2SO4的混合溶液用石墨电极电解一段时间,测得溶液的pH变为b(假设溶液体积的变化忽略不计),在整个电解过程中始终发现只有一个电极有气体产生.下列说法错误的是( )
| A、若使溶液恢复到电解前的浓度可以向溶液中加20(10-b-10-a) g CuCO3 |
| B、?b<a<7 |
| C、阳极电极反应:2H2O-4e-═O2↑+4H+ |
| D、整个过程中是阳极产生氧气,阴极析出铜单质 |

 ,满足上述条件的除A外还有
,满足上述条件的除A外还有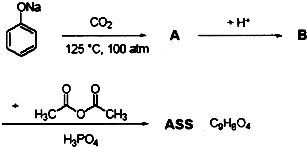
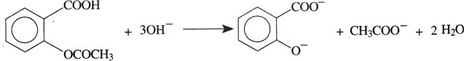
 耗NaOH溶液的体积,分别计算乙酰水杨酸的质量分数.在上述测定过程中,为防止乙酰水杨酸在滴定过程中水解,应如何正确操作?并说明理由.
耗NaOH溶液的体积,分别计算乙酰水杨酸的质量分数.在上述测定过程中,为防止乙酰水杨酸在滴定过程中水解,应如何正确操作?并说明理由.