题目内容
5.下列有关事故的处理措施不正确的是( )| A. | 被浓NaOH溶液灼伤后,先用大量水冲洗,再用醋酸溶液冲洗 | |
| B. | 因吸入溴蒸汽而引起中毒时,可吸入适量的乙醇和乙醚的混和气体解毒 | |
| C. | 皮肤沾有苯酚时,立即用乙醇擦洗 | |
| D. | 吸入了一氧化碳而有中毒症状,赶快到空气新鲜且流通的地方 |
分析 A.醋酸可与氢氧化钠发生中和反应;
B.乙醇、乙醚不能除去溴;
C.苯酚易溶于乙醇;
D.空气新鲜的地方,氧气浓度大.
解答 解:A.醋酸可与氢氧化钠发生中和反应,可降低氢氧化钠对人体的损害,故A正确;
B.乙醇、乙醚不能除去溴,不能排除对人体的损害,故B错误;
C.苯酚易溶于乙醇,可用于除杂苯酚,故C正确;
D.空气新鲜的地方,氧气浓度大,有利于血红蛋白和氧气结合,故D正确.
故选B.
点评 本题考查较为综合,涉及物质的分离、提纯以及实验安全等知识,为高考常见题型,侧重于学生的分析、实验能力的考查,注意把握物质的性质以及实验的操作方法,难度不大.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
20.下列说法中正确的是( )
| A. | 同周期元素的原子电子层数相同 | |
| B. | (长式)元素周期表是按相对原子质量逐渐增大的顺序从左到右排列的 | |
| C. | 最外层电子数相同的元素都是同一族的元素 | |
| D. | 同一主族元素的原子最外层电子数一定相同 |
14.下列叙述I和II均正确并有因果关系的是( )
| 选项 | 叙述I | 叙述II |
| A | Na在Cl2中燃烧的生成物含离子键 | NaCl固体可导电 |
| B | 原电池可将化学能转化为电能 | 原电池需外接电源才能工作 |
| C | 乙烯可与KMnO4溶液发生反应 | 乙烯具有还原性 |
| D | 乙醇的沸点比乙酸的沸点高 | 乙醇和乙酸可通过蒸馏初步分离 |
| A. | A | B. | B | C. | C | D. | D |
15.实验室中不可用于制取NH3的有( )
| A. | 加热浓氨水 | B. | 生石灰和浓氨水 | ||
| C. | Ca(OH)2和NH4Cl共热 | D. | 用氢气和氮气催化合成 |



 或
或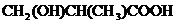 或
或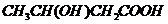 或
或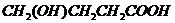


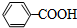
 .
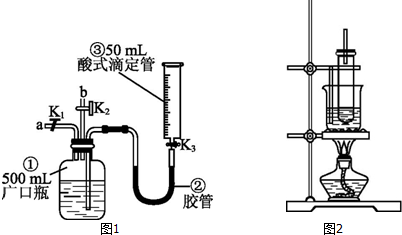
.
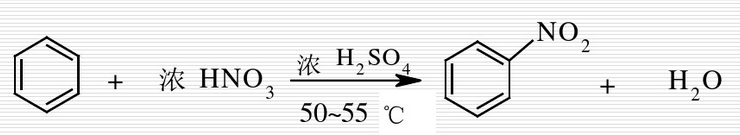 ;
;