题目内容
(8分)为测定某氧化物(化学式为MO)中M是何种金属,做以下实验:称取该氧化物8.0g溶于适量的稀硫酸中,再配制成250.0mL溶液。取该溶液50.0mL用惰性电极进行电解,当刚好电解完全时,电极析出M 1.28g 。通过计算回答以下问题:
(1)M是什么金属?
(2)最初配制的溶液中,该金属离子物质的量浓度是多少?
(3)若50mL此电解液在电解后体积变为40mL,此时溶液的c(H+)是多少?
(8分)⑴ Cu……………………( 3分 )
⑵原溶液中Cu2+=0.4 mol/L……………………( 3分 )
⑶c(H+)=1 mol/L…………………… ( 2分 )
【解析】
试题分析:(1)氧化物8.0g溶于适量的稀硫酸中,再配制成250.0mL溶液,取该溶液50.0mL用惰性电极进行电解,则50mL溶液中氧化物的质量相当于是8.0g/5=1.6g,电极析出M 1.28g,则1.6g该氧化物MO中O元素的质量是1.6g-1.28g=0.32g,所以则1.6gMO中O元素的物质的量是0.32g/16g/mol=0.02mol,即1.6gMO的物质的量是0.02mol,所以MO的摩尔质量是1.6g/0.02mol=80g/mol,数值上=16+M的相对原子质量,所以M的相对原子质量是64,所以M是金属Cu;
(2)8.0gCuO的物质的量是8.0g/80g/mol=0.1mol,所以最初配制的溶液中,Cu2+离子物质的量浓度是0.1mol/0.25L=0.4mol/L;
(3)根据电解硫酸铜的离子方程式2Cu2++2H2O 2Cu+O2↑+4H+,生成1.28gCu,物质的量是1.28g/64g/mol=0.02mol,则生成的氢离子的物质的量是n(H+)=2n(Cu)=0.04mol,所以此时溶液的c(H+)=0.04mol/0.04L=1mol/L。
2Cu+O2↑+4H+,生成1.28gCu,物质的量是1.28g/64g/mol=0.02mol,则生成的氢离子的物质的量是n(H+)=2n(Cu)=0.04mol,所以此时溶液的c(H+)=0.04mol/0.04L=1mol/L。
考点:考查电解原理的应用与计算,物质的量浓度的计算


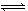 2NO+O2在恒温恒容密闭容器中反应,达到平衡状态的标志是
2NO+O2在恒温恒容密闭容器中反应,达到平衡状态的标志是