题目内容
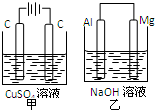 如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,当电路中通过的电子都是0.1mol时,下列说法正确的是( )
如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,当电路中通过的电子都是0.1mol时,下列说法正确的是( )分析:甲中总反应为:2CuSO4+2H2O
2Cu+2H2SO4+O2↑,乙中总反应为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,故甲溶液质量减小,乙溶液质量增大;甲中生成H2SO4,pH减小,乙中消耗NaOH,pH减小;当两装置电路中通过的电子都是0.1
mol时,甲中产生0.025molO2,乙中产生0.05molH2;甲中阴极为Cu2+放电,电极反应为Cu2++2e-=Cu,乙中负极为Al放电,电极反应为:Al-3e-+4OH-=AlO2-+2H2O.
| ||
mol时,甲中产生0.025molO2,乙中产生0.05molH2;甲中阴极为Cu2+放电,电极反应为Cu2++2e-=Cu,乙中负极为Al放电,电极反应为:Al-3e-+4OH-=AlO2-+2H2O.
解答:解:A.甲中总反应为:2CuSO4+2H2O
2Cu+2H2SO4+O2↑,乙中总反应为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,故甲溶液质量减小,乙溶液质量增大,故A正确;
B.甲中生成H2SO4,pH减小,乙中消耗NaOH,pH减小,故B错误;
C.当两装置电路中通过的电子都是0.1mol时,甲中产生0.025molO2,乙中产生0.05molH2,故相同条件下,甲乙中产生气体的体积比为1:2,故C错误;
D.甲中阴极为Cu2+放电,电极反应为Cu2++2e-=Cu,乙中负极为Al放电,电极反应为:Al-3e-+4OH-=AlO2-+2H2O,故D错误.
故选A.
| ||
B.甲中生成H2SO4,pH减小,乙中消耗NaOH,pH减小,故B错误;
C.当两装置电路中通过的电子都是0.1mol时,甲中产生0.025molO2,乙中产生0.05molH2,故相同条件下,甲乙中产生气体的体积比为1:2,故C错误;
D.甲中阴极为Cu2+放电,电极反应为Cu2++2e-=Cu,乙中负极为Al放电,电极反应为:Al-3e-+4OH-=AlO2-+2H2O,故D错误.
故选A.
点评:本题考查原电池和电解池的原理,题目难度中等,易错点为D,注意乙中负极为Al放电,电极反应为:Al-3e-+4OH-=
AlO2-+2H2O,总反应为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
AlO2-+2H2O,总反应为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑.

练习册系列答案
相关题目






