题目内容
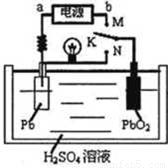
铅蓄电池属于二次电池。下图是铅蓄电池充、放电时的工作示意图,电解质是H2SO4溶液。电池反应为:Pb+PbO2+4H++2SO42— 2PbSO4+2H2O
2PbSO4+2H2O
下列有关说法正确的是
A.实验室用铅蓄电池作电源电解饱和食盐水制取氯气,若制得氯气2.24L,则电池内消耗的H2SO4的物质的量是 0.2mol
B.K与N相接时,H+向正极区迁移
C.K与M连接时,所用电源的b极为负极
D.K与M相接时,阳极附近的pH逐渐增大
【答案】
B
【解析】
试题分析:A、由于铅蓄电池电能和化学能转化时存在损耗,因此当制得2.24L氯气时,消耗硫酸的物质的量至少是0.2mol,错误;B、当K与N相接时,装置为原电池,则H+向正极区迁移,正确;
C、K与M连接时,装置为电解池,b极为正极,错误;D、K与M连接时,阳极发生反应:PbSO4+2H2O -2e= PbO2+4H++SO42-,因此阳极附近pH减小,错误。
考点:本题考查了电化学的知识,要求学生能掌握电极反应方程式的书写和电子转移判断。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
铅蓄电池属于二次电池,其电极材料分别是Pb和PbO2,电解质溶液为一定浓度的硫酸,工作时,该电池的总反应为PbO2+Pb+2H2SO4=2PbSO4+2H2O;PbSO4不溶。
(1)该蓄电池工作时负极的电极反应式为
(2)将质量相等的铁棒和石墨棒分别插入CuSO4溶液中,铁棒接该蓄电池Pb极,石墨棒接该蓄电池PbO2极,一段时间后测得铁棒比石墨棒增加了3.2克,则CuSO4溶液质量 (增加、减少) 克;如果要求将CuSO4溶液恢复成与开始时完全相同,则可以加入下列物质中的
| A.CuSO4溶液 | B.CuCO3固体 | C.CuO固体 | D.Cu(OH)2固体 |
(3)若用该蓄电池作电源(都用惰性材料做电极)电解400克饱和食盐水,如果电池内硫酸的的体积为5升,当其浓度从1.5mol/L降至1.3mol/L时,计算剩余溶液中氯化钠的质量分数(该温度下氯化钠的溶解度为32克)。