题目内容
分别写出下列各小题中阿伏加德罗常数的值,用a、b、c表示。(1)已知a g氧气中含有b个氧原子,则阿伏加德罗常数可表示为___________。
(2)已知标准状况下a L氧气中含有b个氧气分子,则阿伏加德罗常数可表示为____________。
解析:本题主要考查对阿伏加德罗常数与物质的量、气体摩尔体积、物质质量、摩尔质量之间关系的理解。(1)根据n=m/M,a g氧气的物质的量为![]() ,由于氧气是双原子分子,故氧原子的物质的量为
,由于氧气是双原子分子,故氧原子的物质的量为![]() ,因为1 mol物质含有阿伏加德罗常数个粒子,则
,因为1 mol物质含有阿伏加德罗常数个粒子,则![]() =b,即阿伏加德罗常数可表示为16b/a。
=b,即阿伏加德罗常数可表示为16b/a。
(2)根据标准状况下气体摩尔体积的含义,a L氧气的物质的量为![]() ,其所含氧分子数为NAa/22.4个,则b=NAa/22.4,即阿伏加德罗常数可表示为22.4b/a。
,其所含氧分子数为NAa/22.4个,则b=NAa/22.4,即阿伏加德罗常数可表示为22.4b/a。
答案:(1)16b/a (2)22.4b/a

 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案(11分)根据要求完成下列各小题实验目的。
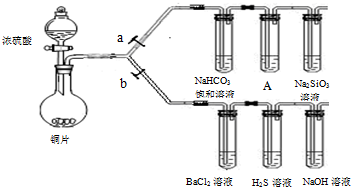
(a、b为弹簧夹,加热及固定装置已略去)
(1)验证碳、硅非金属性的相对强弱。
(已知酸性:亚硫酸>碳酸)
① 连接仪器、 、加药品后,
打开a关闭b,然后滴入浓硫酸,加热。
② 铜与浓硫酸反应的化学方程式是 。
装置A中试剂是 。 ③ 能说明碳的非金属性比硅强的实验现象是 。
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
① 在(1)①操作后打开b,关闭a。② H2S溶液中有浅黄色浑浊出现,化学方程式
是___________________________。
③ BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 |
|
|
写出其中SO2显示还原性生成沉淀的离子方程式___________________________。
(13分)根据要求完成下列各小题实验目的。(a、b为弹簧夹,加热及固定装置已略去)

(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
①连接仪器、检验装置气密性、加药品后,打开a关闭b,然后滴入浓硫酸,加热。
②铜与浓硫酸反应的化学方程式是___________________________。装置A中试剂是________________。
③能说明碳的非金属性比硅强的实验现象是________________________________________________。
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
①在(1)①操作后打开b,关闭a。
②H2S溶液中有浅黄色浑浊出现,化学方程式是______________________________________。
③BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
|
滴加的溶液 |
氯水 |
氨水 |
|
沉淀的化学式 |
|
|
写出其中SO2显示还原性并生成沉淀的离子方程式__________________________________。
④将KOH和Ca(OH)2的混合物1.3g全部溶于一定量水中形成稀溶液,再缓缓通入一定量的B气体,实验过程中可得到沉淀的最大质量为1.2g。
试计算:原混合物中KOH的质量为_____________g。生成沉淀质量为最大时,消耗B气体(标准状况下)的体积(V)范围是:_____________________________________。
(11分)根据要求完成下列各小题实验目的。
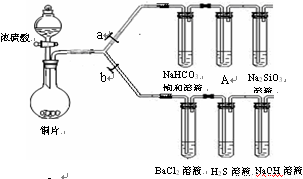
(a、b为弹簧夹,加热及固定装置已略去)
(1)验证碳、硅非金属性的相对强弱。
(已知酸性:亚硫酸>碳酸)
① 连接仪器、 、加药品后,
打开a关闭b,然后滴入浓硫酸,加热。
② 铜与浓硫酸反应的化学方程式是 。
装置A中试剂是 。 ③ 能说明碳的非金属性比硅强的实验现象是 。
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
① 在(1)①操作后打开b,关闭a。② H2S溶液中有浅黄色浑浊出现,化学方程式
是___________________________。
③ BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
|
滴加的溶液 |
氯水 |
氨水 |
|
沉淀的化学式 |
|
|
写出其中SO2显示还原性生成沉淀的离子方程式___________________________。