题目内容
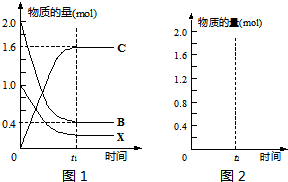
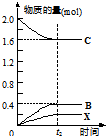
某温度(t ℃)时,水的KW=10-13,则该温度(填“大于”“小于”或“等于”)____________25 ℃,其理由是__________________________________________。将此温度下pH=11的NaOH溶液a L与pH=1的H2SO4的溶液b L混合。
(1)若所得混合液为中性,则a∶b=_______________。
(2)若所得混合液的pH=2,则a∶b=_______________。
大于 水的电离(H2O![]() H++OH-)是吸热过程,升温有利于水的电离,使KW增大
H++OH-)是吸热过程,升温有利于水的电离,使KW增大
(1)10∶1 (2)9∶2
解析:本题主要考查温度对水电离平衡的影响及非常温下溶液的pH计算。解答时应注意溶液为中性的,pH不等于7。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目