��Ŀ����
��(N2H4)ͨ����������ĸ���ȼ�ϣ�N2O4 ������������ش��������⣺
����֪��N2(g)+2O2(g)=2NO2(g) ��H=+a kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g) ��H=-b kJ/mol
2NO2(g) N2O4(g) ��H=-c kJ/mol
N2O4(g) ��H=-c kJ/mol
д����̬������̬ N2O4 ��ȼ�����ɵ�������̬ˮ���Ȼ�ѧ����ʽ ��
�ƹ�ҵ�ϳ��ô�������������İ�����Ӧ�Ʊ��£��÷�Ӧ�Ļ�ѧ����ʽΪ ��
��N2��H2 �ϳɰ���Ϊ���ȷ�Ӧ��800K ʱ��������ʼ�����ͬ���ܱ������г��� 2mol N2��3mol H2�� �������ڷ�Ӧ�����б���ѹǿ���䣬����������������䣬���Ǿ������������������Խ�����ѧƽ�⡣
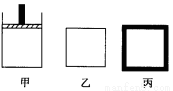
�ﵽƽ��ʱ��ƽ�ⳣ�� K �� K ��(�������������=��)��
�� �ﵽƽ��ʱ N2 ��Ũ�� c(N2)�� c(N2)��(�������������=��)��
�� �Լס��ҡ���������������������˵����ȷ����
A. �����������ܶȲ��ٱ仯ʱ��˵���˷�Ӧ�Ѵﵽƽ��״̬
B. �ڼ��г���ϡ������ He����ѧ��Ӧ���ʼӿ�
C. �����еĻ�������ѹ��ԭ�����һ�룬ƽ�������ƶ�
D.�������¶Ȳ��ٱ仯ʱ˵���Ѵ�ƽ��״̬
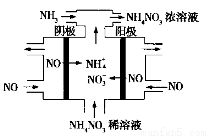
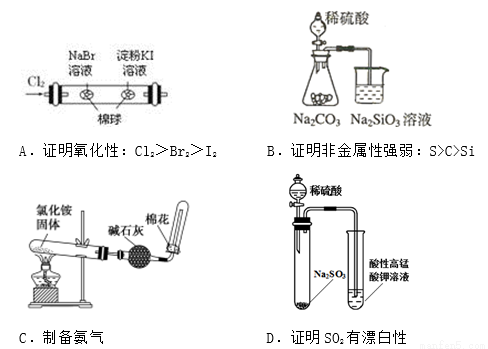
�� ����ͨ����ͼ���װ�ÿ��Ը������� NH4NO3���õ���������ӦʽΪ ��
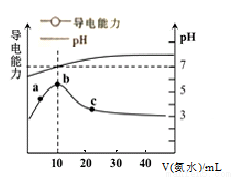
�� �� 20mL 0.2mol/L �� NH4NO3 ��Һ�м��� 10mL 0.2mol/L NaOH ��Һ���Լ��ԣ���Һ����������Ũ�ȴ�С��ϵΪ ��


 B.
B. 
 D.
D. 
 2Z(g)����֪X2��Y2��Z����ʼŨ�ȷֱ�Ϊ0.1 mol��L-1��0.2 mol��L-1��0.2 mol��L-1����һ�������£�����Ӧ�ﵽƽ��ʱ�������ʵ�Ũ���п����� �� ��
2Z(g)����֪X2��Y2��Z����ʼŨ�ȷֱ�Ϊ0.1 mol��L-1��0.2 mol��L-1��0.2 mol��L-1����һ�������£�����Ӧ�ﵽƽ��ʱ�������ʵ�Ũ���п����� �� ��
 ��ɫ����
��ɫ����