题目内容
某校化学兴趣小组同学,利用下列装置探究pH试纸上的微型电解。
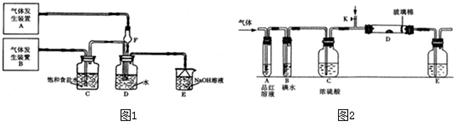
 (1)如图,取一条广泛pH试纸,浸润了饱和Na2SO4溶液后放置于玻璃片上,取两只回形针(铁制)夹住试纸两端,另取导线、鳄鱼夹、6v电池连接好电路。
(1)如图,取一条广泛pH试纸,浸润了饱和Na2SO4溶液后放置于玻璃片上,取两只回形针(铁制)夹住试纸两端,另取导线、鳄鱼夹、6v电池连接好电路。
当两根鳄鱼夹夹住回形针后,试纸上立刻出现以下现象:
|
紫色,对照比色卡发现其pH约为13。
①如图,右端回形针为 极(填“阴”或“阳”);
阴极试纸上出现大片蓝紫色的原因是(用反应式结合文字表示): 。
②推测阳极回形针处出现的红棕色物质可能是 (写化学式),为证明该种物质的存在,请设计一个简单的实验,该实验的操作过程是: 。
 (2)小组同学另取两根铅笔芯作为电极,对pH试纸上的Na2SO4溶液电解,可见阳极与试纸接触处呈现 色圆点,而在阴极与试纸接触处呈现 色圆点,说明了电解硫酸钠饱和溶液的实质是: (用方程式表示)。
(2)小组同学另取两根铅笔芯作为电极,对pH试纸上的Na2SO4溶液电解,可见阳极与试纸接触处呈现 色圆点,而在阴极与试纸接触处呈现 色圆点,说明了电解硫酸钠饱和溶液的实质是: (用方程式表示)。
(3)将pH试纸用饱和NaCl浸润,采用类似(2)操作,如图。接通直流电源一段时间后,发现a电极与试纸接触处出现一个双色同心圆,内圈为白色,外圈呈浅红色。
请分析此极出现该现象的原因:(用必要文字及方程式表述)
(1)①阳 ; 2H+ +2e-→H2↑,使水的电离平衡右移,增大c(OH-)
②氧化铁 (Fe2O3) ;取少许红棕色物质置于试管中,加稀盐酸至完全溶解后,
(发现溶液呈棕黄色,)滴加一滴KSCN溶液振荡,溶液出现血红色,从而证明推测。
(2)红 ;蓝 ; 2H2O ![]() 2H2↑+O2↑
2H2↑+O2↑
(3)a极为阳极,电极反应式为:2Cl-→ Cl2↑+2e- ,氯气溶于水发生反应:
Cl2+H2O ===HClO +HCl ,HClO具有漂白性使pH试纸变白色(内圈);
氯水呈酸性因而外圈出现浅红色。

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案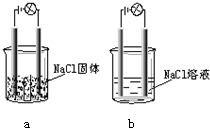 某校化学兴趣小组同学在实验室做实验,按照如图a图连接好线路发现小灯泡不亮,按照如图b图连接好线路发现小灯泡会亮,由此得出的结论正确的是( )
某校化学兴趣小组同学在实验室做实验,按照如图a图连接好线路发现小灯泡不亮,按照如图b图连接好线路发现小灯泡会亮,由此得出的结论正确的是( )| A、NaCl固体是非电解质 | B、NaCl在水中能电离出可以自由移动的离子 | C、NaCl能使溶液中的水电离出大量的离子 | D、NaCl溶液是电解质 |