题目内容
工业上从铝土矿(含氧化铝、氧化铁等)制取铝的流程如图所示: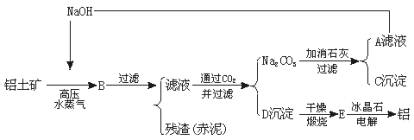
经分析,生产原料(铝土矿)和提取Al2O3后的残渣(赤泥)的部分成分见下表(以氧化物表示)。已知铝土矿中的Fe2O3全部转入赤泥。
|
|
Al2O3 |
Fe2O3 |
Na2O(由NaOH折算成Na2O) |
|
铝土矿 |
55% |
16% |
0% |
|
赤泥 |
15% |
48% |
8% |
(1)生产中每消耗1 t铝土矿将产生多少t赤泥?
(2)试计算出每炼1 t铝,理论上需要多少t铝土矿?应补充多少t NaOH?
答案:
解析:
解析:
答案:解:(1)根据制取铝的流程,从铝土矿到赤泥,氧化铁的质量未变。
设赤泥的质量为x,则:x×48%=1 t×16% x=1/3 t
(2)2Al2O3![]() 4Al+3O2↑
4Al+3O2↑
设需要铝土矿的质量为y,则:(y×55%-y×15%/3)×54/102=1 t
y=3.78 t
Al2O3+2NaOH===2NaAlO2+H2O 2NaAlO2+CO2+3H2O===2Al(OH)3↓+Na2CO3
Na2CO3+Ca(OH)2===CaCO3↓+2NaOH
从反应看,与Al2O3反应的NaOH正是以上反应生成的。应补充的是赤泥中的NaOH,为(3.78 t×8%×2×40/62)/3=0.129 t

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

 某化学兴趣小组模拟工业上从铝土矿(主要成分是
某化学兴趣小组模拟工业上从铝土矿(主要成分是 ,含
,含 、
、 等杂质)中提取氧化铝的工艺做实验,流程如下:
等杂质)中提取氧化铝的工艺做实验,流程如下:
 ,含
,含 、
、 等杂质)中提取氧化铝的工艺做实验,流程如下:
等杂质)中提取氧化铝的工艺做实验,流程如下:
 请回答下列问题:
请回答下列问题: