题目内容
为提纯下列物质(括号内为少量杂质),所选除杂试剂与主要分离方法都正确的是
| | 不纯物质 | 除杂试剂 | 分离方法 |
| A | 苯(甲苯) | KMnO4(酸化),NaOH溶液 | 分液 |
| B | NH4Cl溶液(FeCl3) | NaOH溶液 | 过滤 |
| C | 甲烷(乙烯) | 酸性KMnO4溶液 | 洗气 |
| D | 苯(苯酚) | 浓溴水 | 过滤 |
A
解析试题分析:A、甲苯能被高锰酸钾氧化为苯甲酸,再与NaOH反应后与苯分层,然后分液可除杂,故A正确;B、二者均与NaOH反应,不能除杂,应加氨水反应后过滤除杂,故B错误;C、乙烯被高锰酸钾氧化生成二氧化碳,引入新杂质,应加溴水,然后洗气除杂,故C错误;D、溴、溴苯均易溶于苯,不能除杂,应加NaOH反应后分液来除杂,故D错误。
考点:本题考查混合物的分离、提纯。

练习册系列答案
相关题目
孔雀石主要含Cu2(OH)2CO3,还含少量Fe的氧化物和SiO2,实验室以孔雀石为原料制备CuSO4·5H2O及CaCO3,步骤如下: 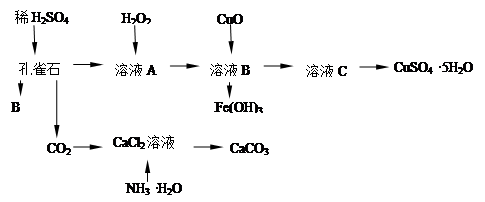
试回答下列问题:
(1)B物质的化学式是 在未加入H2O2的溶液中,存在的金属离子有Cu2+、Fe2+、Fe3+。若检验该溶液中Fe3+,选择最合适的试剂是 (填代号)。
| A.KMnO4溶液 | B.Fe粉 | C.Na2CO3溶液 | D.KSCN溶液 |
(3)由溶液C获得CuSO4·5H2O,需要经过 ,过滤等操作。除烧杯、漏斗外,过滤操作还需用到另一玻璃仪器是 。
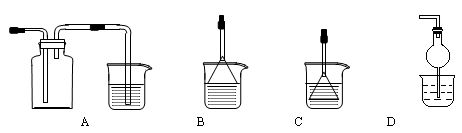
(4)制备CaCO3时,先通入 (填NH3或CO2),若实验过程中有氨气逸出,可选用下列装置中的 (填代号)装置吸收氨气。(烧杯中的液体都为水)
下列除去杂质的方法,正确的是
| A.苯中含有苯酚杂质:加入溴水,过滤 |
| B.乙醇中含有乙酸杂质:加入碳酸钠溶液,分液 |
| C.FeCl3溶液中含有CuCl2杂质:加入过量铁粉,过滤 |
| D.CO2中含有HCl杂质:通入饱和NaHCO3溶液,洗气 |
.现有三组混合液:①乙酸乙酯和乙酸钠水溶液;②乙醇和丁醇;③溴化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
| A.分液、萃取、蒸馏 | B.萃取、蒸馏 、分液 |
| C.分液、蒸馏、萃取 | D.蒸馏、萃取、分液 |
只用一种试剂鉴别正己烷、1-己烯、乙醇、苯酚水溶液4种无色液体,应选用
| A.酸性KMnO4溶液 | B.饱和溴水 | C.NaOH溶液 | D.AgNO3溶液 |
下列实验中,所选装置不合理的是 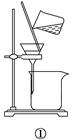




| A.分离Na2CO3溶液和CH3COOC2H5,选④ |
| B.用CCl4提取碘水中的碘,选③ |
| C.用FeCl2溶液吸收Cl2,选⑤ |
| D.粗盐提纯,选①和② |
海洋约占地球表面积的71%,对其进行开发利用的部分流程如图所示。下列说法错误的是( )
| A.试剂1可以选用石灰乳 |
| B.从苦卤中提取Br2的反应的离子方程式为:2Br - + Cl2=2Cl- + Br2 |
| C.工业上,电解熔融MgO冶炼金属镁可减小能耗 |
| D.可用BaCl2溶液除去粗盐中的SO42- |
