题目内容
【题目】在碱性条件下使用鸟粪石[Mgx(NH4)y(PO4)z·nH2O]处理氨氮废水具有加热时间短,氨逸出彻底等优点。反应原理如下:
yNa++yOH-+Mgx(NH4)y(PO4)z·nH2O![]() Mgx(Na)y(PO4)z+yNH3↑+(n+y)H2O
Mgx(Na)y(PO4)z+yNH3↑+(n+y)H2O
Mgx(Na)y(PO4)z+y![]() +nH2O
+nH2O![]() yNa++Mgx(NH4)y(PO4)z·nH2O↓
yNa++Mgx(NH4)y(PO4)z·nH2O↓
(1)上述氨氮废水处理过程中鸟粪石所起的作用是__________。
(2)其它条件不变,若鸟粪石化学式中的z保持不变,x越大,处理相同量的氨氮废水所需的时间就_________(填:“越长”“越短”“不变”)。
(3)为测定鸟粪石的组成,进行下列实验:
①取鸟粪石2.45 g与足量的NaOH溶液混合,加热,收集到标准状况下的气体224mL
②另取鸟粪石2.45 g溶于稍过量盐酸,用蒸馏水配成100.00 mL溶液A;
③取25.00 mL溶液A,调节pH=10,用浓度为0.1000 mol·L-1的EDTA标准溶液滴定Mg2+,滴定至终点,消耗EDTA标准溶液25 mL(已知Mg2+与EDTA反应的化学计量比1∶1);
④取25.00 mL溶液A,加入0.005mol的BiCl3,调节溶液pH生成Mg3(PO4)2和BiPO4沉淀,过滤,滤液中的Bi3+用EDTA标准溶液滴定为![]() mol。通过计算确定鸟粪石的化学式_____________(写出计算过程)。
mol。通过计算确定鸟粪石的化学式_____________(写出计算过程)。
【答案】催化剂 越长 n(![]() )=n(NH3)=
)=n(NH3)=![]() =0.01mol
=0.01mol
n(Mg2+)=n(EDTA)×![]() =0.1000 mol·L-1×25.00 mL×10-3×
=0.1000 mol·L-1×25.00 mL×10-3×![]() =0.01mol
=0.01mol
n(![]() )=0.01mol×
)=0.01mol×![]() +(0.005mol-
+(0.005mol-![]() mol)×4=0.01mol
mol)×4=0.01mol
n(H2O)=![]() =0.06mol
=0.06mol
n(![]() ):n(Mg2+):n(
):n(Mg2+):n(![]() ):n(H2O)=0.01mol:0.01mol:0.01mol:0.06mol=1:1:1:6
):n(H2O)=0.01mol:0.01mol:0.01mol:0.06mol=1:1:1:6
故鸟粪石的化学式为MgNH4PO4·6H2O
【解析】
根据所给方程式判断鸟粪石在反应中的作用;根据定量分析中所给出的数据计算各粒子的物质的量,随后根据各粒子的物质的量的比确定鸟粪石的化学式。
(1)将上述两个方程式相加得![]() +OH-=NH3↑+H2O,说明第一个反应消耗多少鸟粪石第二个反应就生成多少鸟粪石,故鸟粪石在处理氨氮废水的过程中起到催化剂的作用;
+OH-=NH3↑+H2O,说明第一个反应消耗多少鸟粪石第二个反应就生成多少鸟粪石,故鸟粪石在处理氨氮废水的过程中起到催化剂的作用;
(2)根据鸟粪石化学式[Mgx(NH4)y(PO4)z·nH2O],当z保持不变,x越大时,鸟粪石中铵根含量降低,可以处理的氨氮废物的量减小,处理相同量的氨氮废水所需的时间就越长;
(3)n(![]() )=n(NH3)=
)=n(NH3)=![]() =0.01mol
=0.01mol
n(Mg2+)=n(EDTA)×![]() =0.1000 mol·L-1×25.00 mL×10-3×
=0.1000 mol·L-1×25.00 mL×10-3×![]() =0.01mol
=0.01mol
n(![]() )=0.01mol×
)=0.01mol×![]() +(0.005mol-
+(0.005mol-![]() mol)×4=0.01mol
mol)×4=0.01mol
n(H2O)=![]() =0.06mol
=0.06mol
n(![]() ):nspan>(Mg2+):n(
):nspan>(Mg2+):n(![]() ):n(H2O)=0.01mol:0.01mol:0.01mol:0.06mol=1:1:1:6
):n(H2O)=0.01mol:0.01mol:0.01mol:0.06mol=1:1:1:6
故鸟粪石的化学式为MgNH4PO4·6H2O。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】广东河源市东源县某村土壤的主要成份是Al2O3、Fe3O4及SiO2,广州大学附属东江中学“探险号”化学兴趣小组设计以下流程提取金属铝:
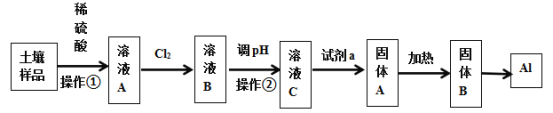
信息提示:氧化铝在电解条件下可得金属铝;Fe(OH)3、Al(OH)3、Fe(OH)2开始沉淀与完全沉淀的pH数据表:
Fe(OH)3 | Al(OH)3 | Fe(OH)2 | |
开始沉淀的pH | 2.7 | 3.3 | 5.9 |
完全沉淀的pH | 3.2 | 5.2 | 8.4 |
(1)溶液A含有的金属阳离子为_________________固体B的化学式为_______________________
(2)步骤中通入氯气时的离子方程式为___________________________________________________
(3)溶液C的pH范围是_____________________,操作②的名称是_________________________
(4)通入试剂a的离子方程式为_________________________________________________________