��Ŀ����
��4 mol A�����2 mol B������2 L�������л�ϲ���һ�������·������·�Ӧ��2A(g)+B(g) 2C(g)������2 s����C��Ũ��Ϊ0.6 mol��L-1���������м���˵����
2C(g)������2 s����C��Ũ��Ϊ0.6 mol��L-1���������м���˵����
��������A��ʾ�ķ�Ӧƽ������Ϊ0.3 mol��L-1��s-1
��������B��ʾ�ķ�Ӧ��ƽ������Ϊ0.6 mol��L-1��s-1
��2sʱ����A��ת����Ϊ70%
��2sʱ����B��Ũ��Ϊ0.7 mol��L-1
������ȷ����
A���٢� B���٢�
C���ڢ� D���ۢ�
���𰸡�
B
��������
�������������A��B��Ũ�ȷֱ�Ϊ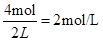 ��
��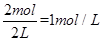
2A(g)+B(g) 2C(g)
2C(g)
��ʼ��mol/L���� 2 1 0
�仯��mol/L���� 0.6 0.3 0.6
ƽ�⣨mol/L���� 1.4 0.7 0.6
��������A��ʾ�ķ�Ӧƽ������Ϊ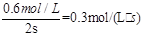
��������B��ʾ�ķ�Ӧ��ƽ������Ϊ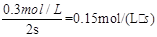
��2sʱ����A��ת����Ϊ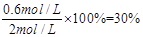
��2sʱ����B��Ũ��Ϊ0.7 mol��L-1
�ʴ�ѡB��
���㣺��Ӧ���ʡ�ת���ʵļ���
������������Ҫ�����˷�Ӧ���ʼ�ת���ʵļ��㡣����ҪӦ�á�����ʽ����������⣬��Ӧ���ʵļ��㹫ʽ��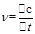 ��ת���ʵļ��㹫ʽ��
��ת���ʵļ��㹫ʽ��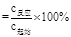

��ϰ��ϵ�д�
�����Ŀ
 ���� 2 s���� C �����ʵ���Ũ��Ϊ 0.6 mol��L-1���������м���˵����
���� 2 s���� C �����ʵ���Ũ��Ϊ 0.6 mol��L-1���������м���˵����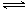 2C��g��,���� 2 s���룩����C ��Ũ��Ϊ 0.6 mol��L��1 ����
������ A ��ʾ�ķ�Ӧ��ƽ������
�� 2 s ʱ���� B ��Ũ��Ϊ
��
2C��g��,���� 2 s���룩����C ��Ũ��Ϊ 0.6 mol��L��1 ����
������ A ��ʾ�ķ�Ӧ��ƽ������
�� 2 s ʱ���� B ��Ũ��Ϊ
�� 2C(g)����2s ����C��Ũ��Ϊ0.6mol•L-1�������м���˵�����в���ȷ����
2C(g)����2s ����C��Ũ��Ϊ0.6mol•L-1�������м���˵�����в���ȷ����  2C��g������2 s ����C��Ũ��Ϊ0.6 mol/L�����м���˵����ȷ����
2C��g������2 s ����C��Ũ��Ϊ0.6 mol/L�����м���˵����ȷ����