题目内容
由CO2、H2O(g)组成的混合气体共a mol,其中CO2的物质的量分数为x.将该混合气体缓慢通过装有1mol Na2O2的真空管,充分反应后,维持120℃、1.01×105Pa.收集所得气体,冷却、称量,真空管中固体质量增加y g.
(1)若a=1,则y=______(用含x代数式表示);
(2)若a=2,x=0.5时,反应后所得气体的成份是______;
(3)若a=2,y=28时,则x的取值范围______;
(4)若a=1.25,试在图中作出y与x的关系曲线,并在y轴标明曲线起点和终点的数值.
解:(1)由反应2CO2+2Na2O2=2Na2CO3+O2,2H2O+2Na2O2=4NaOH+O2↑可知,气体与过氧化钠都按1:1反应,a=1时,混合气体与过氧化钠恰好反应,n(CO2)=ax=x,固体增重为y=28n(CO2)+2[1-n(CO2)]=28x+2(1-x)=26x+2,故答案为:26x+2;
(2)a=2,x=0.5时,n(CO2)=1mol,二氧化碳与过氧化钠恰好反应,水不反应,从Na2O2的真空管出来的气体有氧气、水蒸气,故答案为:氧气、水;
(3)a=2,y=28时,若x≥0.5,水不参加反应,根据过氧化钠计算增重为y=28n(Na2O2)=28,故0.5≤x<1,固体增重28g;
若<0.5,二氧化碳完全反应,参加反应的水为[1-n(CO2)]mol,所以固体增重为y=28n(CO2)+2[1-n(CO2)]=28×2x+2(1-2x)=28,解得x=2,不符合题意,
故答案为:0.5≤x<1;
(4)当a=1.25时,若x≥0.8,水不参加反应,根据过氧化钠计算增重为y=28n(Na2O2)=28;
若x<0.8,二氧化碳完全反应,参加反应的水为[1-n(CO2)]mol,所以固体增重为y=28n(CO2)+2[1-n(CO2)]=28×2x+2(1-2x)=52x+2,当x=0时中含有氢气,y=2,y与x的关系曲线图为:
 ,故答案为:
,故答案为: .
.
分析:一定量的CO2、H2O(g)组成的混合气体与过氧化钠反应,可以看做CO2先与过氧化钠反应,CO2反应完毕,H2O(g)再与过氧化钠反应,发生反应2CO2+2Na2O2=2Na2CO3+O2,固体增加的质量相当于与二氧化碳等物质的量的CO的质量,2H2O+2Na2O2=4NaOH+O2↑,固体增加的质量为相当于与水等物质的量的H2的质量,根据过氧化钠的物质的量讨论二氧化碳恰好反应时x的值,根据x的值分情况讨论,以此解答.
(1)a=1时,混合气体与过氧化钠恰好反应;
(2)a=2,x=0.5时,n(CO2)=1mol,二氧化碳与过氧化钠恰好反应,水不反应;
(3)a=2,y=28时,若x≥0.5,水不参加反应,根据过氧化钠计算增重为y=28n(Na2O2),若<0.5,二氧化碳完全反应,参加反应的水为[1-n(CO2)]mol,所以固体增重为y=28n(CO2)+2[1-n(CO2)];
(4)当a=1.25时,若x≥0.8,水不参加反应,根据过氧化钠计算增重为y=28n(Na2O2),若x<0.8,二氧化碳完全反应,参加反应的水为[1-n(CO2)]mol,所以固体增重为y=28n(CO2)+2[1-n(CO2)];
过氧化钠不足量,采用极限法确定y与x的关系曲线,当气体全部为氢气时,计算y的质量,当气体全部为二氧化碳时,计算y的质量.
点评:本题考查混合物的计算,难度中等,将反应设计为CO2先与过氧化钠反应,CO2反应完毕,H2O(g)再与过氧化钠反应是解题的关键,再判断二氧化碳恰好反应计算x的值,进行讨论.
(2)a=2,x=0.5时,n(CO2)=1mol,二氧化碳与过氧化钠恰好反应,水不反应,从Na2O2的真空管出来的气体有氧气、水蒸气,故答案为:氧气、水;
(3)a=2,y=28时,若x≥0.5,水不参加反应,根据过氧化钠计算增重为y=28n(Na2O2)=28,故0.5≤x<1,固体增重28g;
若<0.5,二氧化碳完全反应,参加反应的水为[1-n(CO2)]mol,所以固体增重为y=28n(CO2)+2[1-n(CO2)]=28×2x+2(1-2x)=28,解得x=2,不符合题意,
故答案为:0.5≤x<1;
(4)当a=1.25时,若x≥0.8,水不参加反应,根据过氧化钠计算增重为y=28n(Na2O2)=28;
若x<0.8,二氧化碳完全反应,参加反应的水为[1-n(CO2)]mol,所以固体增重为y=28n(CO2)+2[1-n(CO2)]=28×2x+2(1-2x)=52x+2,当x=0时中含有氢气,y=2,y与x的关系曲线图为:
 ,故答案为:
,故答案为: .
.分析:一定量的CO2、H2O(g)组成的混合气体与过氧化钠反应,可以看做CO2先与过氧化钠反应,CO2反应完毕,H2O(g)再与过氧化钠反应,发生反应2CO2+2Na2O2=2Na2CO3+O2,固体增加的质量相当于与二氧化碳等物质的量的CO的质量,2H2O+2Na2O2=4NaOH+O2↑,固体增加的质量为相当于与水等物质的量的H2的质量,根据过氧化钠的物质的量讨论二氧化碳恰好反应时x的值,根据x的值分情况讨论,以此解答.
(1)a=1时,混合气体与过氧化钠恰好反应;
(2)a=2,x=0.5时,n(CO2)=1mol,二氧化碳与过氧化钠恰好反应,水不反应;
(3)a=2,y=28时,若x≥0.5,水不参加反应,根据过氧化钠计算增重为y=28n(Na2O2),若<0.5,二氧化碳完全反应,参加反应的水为[1-n(CO2)]mol,所以固体增重为y=28n(CO2)+2[1-n(CO2)];
(4)当a=1.25时,若x≥0.8,水不参加反应,根据过氧化钠计算增重为y=28n(Na2O2),若x<0.8,二氧化碳完全反应,参加反应的水为[1-n(CO2)]mol,所以固体增重为y=28n(CO2)+2[1-n(CO2)];
过氧化钠不足量,采用极限法确定y与x的关系曲线,当气体全部为氢气时,计算y的质量,当气体全部为二氧化碳时,计算y的质量.
点评:本题考查混合物的计算,难度中等,将反应设计为CO2先与过氧化钠反应,CO2反应完毕,H2O(g)再与过氧化钠反应是解题的关键,再判断二氧化碳恰好反应计算x的值,进行讨论.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
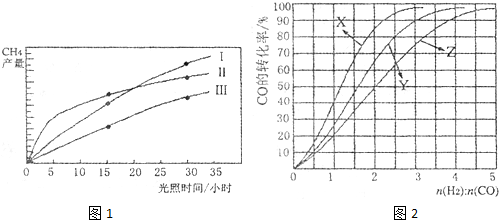
 (2011?广东)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2.紫外光照射时,在不同催化剂(I,II,III)作用下,CH4产量随光照时间的变化如图所示.
(2011?广东)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2.紫外光照射时,在不同催化剂(I,II,III)作用下,CH4产量随光照时间的变化如图所示.