题目内容
(1)有四种短周期元素的部分性质如下(气体密度已换算为标准状况):
则W、X、Y、Z四种元素的第一电离能由大到小的顺序是: (用元素符号表示).
(2)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途.富勒烯(C60)的结构如图2,1mol C60分子中σ键的数目为 .
(3)根据等电子体原理,写出一种与SO3互为等电子体的分子的分子式 .
(4)某配合物的分子结构如图2所示,则C原子的杂化方式为 ;基态Ni原子的电子排布式 .
(5)乙酸熔沸点较高,是由于存在以分子间氢键缔合的二聚体(含一个环状结构),请画出这二聚体的结构:
.

| 元素 | W | X | Y | Z |
| 原子半径 | 186pm | 75pm | 66pm | 77pm |
| 核外电子 | 有4种能级不同的电子 | 最外层有5种运动状态不同的电子 | 核外电子占有5个轨道 | 有2个未成对电子 |
| 单质部分性质 | 密度:0.97g?cm-3 熔点:97.8℃ 能导电 |
沸点:-196.0℃不能导电 | 密度:1.43g?L-1 沸点:-183.0℃ 不能导电 |
熔点:3550℃ 能导电 |
(2)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途.富勒烯(C60)的结构如图2,1mol C60分子中σ键的数目为
(3)根据等电子体原理,写出一种与SO3互为等电子体的分子的分子式
(4)某配合物的分子结构如图2所示,则C原子的杂化方式为
(5)乙酸熔沸点较高,是由于存在以分子间氢键缔合的二聚体(含一个环状结构),请画出这二聚体的结构:

考点:原子核外电子排布,元素电离能、电负性的含义及应用,“等电子原理”的应用,原子轨道杂化方式及杂化类型判断
专题:原子组成与结构专题,化学键与晶体结构
分析:(1)W、X、Y、Z为短周期元素,W原子有4种能级不同的电子,应为1s22s22p63s1或1s22s22p63s2,能导电,密度小于水,沸点较低,W应为钠元素;
Y原子核外电子占有5个轨道,应为1s22s22pn,3≤n≤6,单质沸点:-183.0℃,为气体,密度为1.43g?L-1,单质摩尔质量为1.43g?L-1×22.4L/mol=32,故Y为氧元素;
X最外层有5种运动状态不同的电子,处于ⅤA族,原子半径大于氧元素,故X为氮元素;
Z原子有2个未成对电子,原子半径小于氯元素,Z应处于第二周期,外围电子排布为2s22p2或2s22p4,单质熔点:3550℃,能导电,则Z为碳元素;
同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第IIA族、第VA族元素的第一电离能大于相邻元素,金属性越强第一电离能越小;
(2)利用均摊法计算每个碳原子含有几个σ键,从而计算1mol C60分子中σ键的数目;
(3)具有相同原子数和价电子数的微粒互称为等电子体;
(4)由图2可知,结构中含有两种C原子,位于甲基上、C=N中C原子,根据结构确定σ键,进而确定杂化轨道数目,确定杂化方式;根据能量最低原理书写电子排布式;
(5)在二个乙酸分子间中,羧基上的氢原子与另一个乙酸分子中碳氧双键上氧原子形成氢键.
Y原子核外电子占有5个轨道,应为1s22s22pn,3≤n≤6,单质沸点:-183.0℃,为气体,密度为1.43g?L-1,单质摩尔质量为1.43g?L-1×22.4L/mol=32,故Y为氧元素;
X最外层有5种运动状态不同的电子,处于ⅤA族,原子半径大于氧元素,故X为氮元素;
Z原子有2个未成对电子,原子半径小于氯元素,Z应处于第二周期,外围电子排布为2s22p2或2s22p4,单质熔点:3550℃,能导电,则Z为碳元素;
同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第IIA族、第VA族元素的第一电离能大于相邻元素,金属性越强第一电离能越小;
(2)利用均摊法计算每个碳原子含有几个σ键,从而计算1mol C60分子中σ键的数目;
(3)具有相同原子数和价电子数的微粒互称为等电子体;
(4)由图2可知,结构中含有两种C原子,位于甲基上、C=N中C原子,根据结构确定σ键,进而确定杂化轨道数目,确定杂化方式;根据能量最低原理书写电子排布式;
(5)在二个乙酸分子间中,羧基上的氢原子与另一个乙酸分子中碳氧双键上氧原子形成氢键.
解答:
解:(1)W应为钠元素;Y为氧元素;X为氮元素;Z为碳元素;同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第IIA族、第VA族元素的第一电离能大于相邻元素,金属性越强第一电离能越小,故第一电离能:N>O>C>Na;
故答案为:N>O>C>Na;
(2)每个碳原子含有的σ键个数为3×
,所以1mol C60分子中σ键的数目=
NA=90NA;
故答案为:90NA;
(3)与SO3的原子数为4,价电子数为24,与与SO3互为等电子体的分子的分子式BF3;
故答案为:BF3;
(4)由图2可知,结构中含有两种C原子,位于甲基上、C=N中C原子,甲基中C原子成3个C-H、1个C-C,故杂化轨道数目为4,采取sp3杂化,C=N中C原子成2个C-C、1个C=N,杂化轨道数目为3,采取sp2杂化;Ni的原子序数为28,电子排布式为[Ar]3d84s2,
故答案为:sp2、sp3;[Ar]3d84s2.
(5)二个乙酸分子间中,羧基上的氢原子与另一个乙酸分子中碳氧双键上氧原子形成氢键,所以其氢键表示为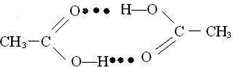 ,
,
故答案为: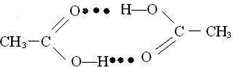 .
.
故答案为:N>O>C>Na;
(2)每个碳原子含有的σ键个数为3×
| 1 |
| 2 |
| 3 |
| 2 |
故答案为:90NA;
(3)与SO3的原子数为4,价电子数为24,与与SO3互为等电子体的分子的分子式BF3;
故答案为:BF3;
(4)由图2可知,结构中含有两种C原子,位于甲基上、C=N中C原子,甲基中C原子成3个C-H、1个C-C,故杂化轨道数目为4,采取sp3杂化,C=N中C原子成2个C-C、1个C=N,杂化轨道数目为3,采取sp2杂化;Ni的原子序数为28,电子排布式为[Ar]3d84s2,
故答案为:sp2、sp3;[Ar]3d84s2.
(5)二个乙酸分子间中,羧基上的氢原子与另一个乙酸分子中碳氧双键上氧原子形成氢键,所以其氢键表示为
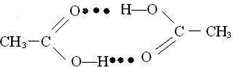 ,
,故答案为:
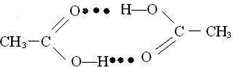 .
.
点评:本题考查较综合,涉及氢键、第一电离能、化学键、原子杂化、电子排布式的书写等知识点,难点是氢键的书写,明确哪些元素的原子能形成氢键,难度中等.

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案
相关题目
下列各组物质,属于同分异构体的是( )
A、 和 和 |
B、 和H3C-CH2-NO2 和H3C-CH2-NO2 |
| C、H3C-CH2-CH2-COOH和H3C-CH2-CH2-CH2-COOH |
D、H3C-CH2-O-CH2-CH3和 |
分析化学反应:3 Cu2S+16HNO3═6Cu(NO3)2+4NO+3S+8H2O,下列说法不正确的是( )
| A、只有硫元素被氧化 |
| B、NO是还原产物 |
| C、还原剂与氧化剂的物质的量之比是3:16 |
| D、0.3mol Cu(NO3)2生成时转移电子0.6mol |
 ,请完成下列问题:
,请完成下列问题: