题目内容
已知反应:4NH3+5O2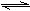 4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列关系表示正确的是 ()。
4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列关系表示正确的是 ()。A.5v(NH3)/6=v(O2) B.5v(O2)/6=v(H2O)
C.2v(NH3)/2=v(H2O) D.4v(O2)/5=v(NO)
D
【试题分析】

练习册系列答案
相关题目
题目内容
已知反应:4NH3+5O2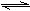 4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列关系表示正确的是 ()。
4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列关系表示正确的是 ()。