题目内容
已知氯水中有以下平衡:Cl2+H2O![]() HCl+HClO,常温下,用50 mL的针筒吸入40 mL氯气后,再吸进10 mL水.
HCl+HClO,常温下,用50 mL的针筒吸入40 mL氯气后,再吸进10 mL水.
(1)写出针筒中可观察到的现象.
(2)若将针筒长时间放置,又可能看到何种变化?试用平衡观点加以解释.
答案:
解析:
解析:
|
答案:(1)气体体积缩小,溶液呈浅黄绿色. (2)气体体积进一步缩小,气体和溶液均变成无色.氯水中存在平衡Cl2+H2O 思路解析:从Cl2与水反应产生的HCl和HClO溶于水,及HClO见光易分解,从而引起Cl2+H2O |

练习册系列答案
相关题目
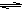 HCl+HClO,CaCO3与氯水中的HCl反应,使c(H+)减小,平衡向右移动,HClO浓度增大,故漂白性增强
HCl+HClO,CaCO3与氯水中的HCl反应,使c(H+)减小,平衡向右移动,HClO浓度增大,故漂白性增强